Другой изотоп
Cтраница 2
При такой ширине линии испускания поглощение ее компонентами, принадлежащими другим изотопам, практически исключено. [16]
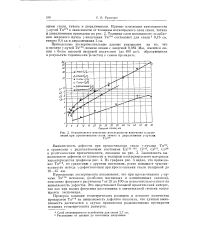 |
Относительное изменение интенсивности излучения и экспозиций при просвечивании стали, титана и дюралюминия т-лучами. [17] |
Из графика рис. 3 видно, что применение Ти170, по сравнению с другими изотопами, резко повышает чувствительность метода у-дефектоскопии При просвечивании стали толщиной до 10 - 15 мм. [18]
Осадок гексани-трородиата калия затем растворяется в царской водке, и для очистки родия от загрязнений другими изотопами вводятся носители цирконий и серебро, которые затем осаждаются добавлением фениларсоновой и соляной кислот. [19]
При этом процессе заряд ядра не изменяется; следовательно, образуется не новый элемент, а другой изотоп. Эта реакция возникает со значительным выходом уже при относительно низких энергиях падающих дейтронов. Она нередко встречается и у самых тяжелых элементов. Гамова приводит к вероятностям превращения, гораздо меньшим, чем те, ко - торые наблюдаются в действительности. Особенно непонятными кажутся превращения наиболее тяжелых элементов при энергиях дейтронов, выражаемых небольшим числом MeV. Для этого типа реакции приходится составить себе другую картину. Как уже было сказано, при ( d, р) - процессе заряд ядра не изменяется. Таким образом, при столкновении происходит простой обмен нейтроном; поскольку нейтрон не имеет заряда, то ему не нужно преодолевать потенциального барьера, чтобы попасть в ядро. На основе этого представления становится понятно, что реакция типа ( d, р) протекает с большим выходом уже при сравнительно низких энергиях дейтронов. Криш-нана и Нахума) ход эффективного сечения для ( d, n) - и ( d, p) - процессов на тяжелых ядрах. [20]
Поэтому часто принимают, что химические свойства веществ не меняются при замене в них одного изотопа на другой изотоп того же элемента. Строго говоря, это не совсем так. Чем больше относительная разница в массах изотопов, тем сильнее различаются физические и химические свойства соответствующих веществ. [21]
Вследствие огромной относительной разницы в их атомных массах ( масса атома одного изотопа вдвое больше массы атома другого изотопа) свойства этих изотопов заметно различаются. Изотоп водорода с массовым числом 2 называют дейтерием и обозначают символом D. [22]
Простейшим типом точечного дефекта является атом изотопа элемента, расположенный з узле решетки, состоящей из атомов другого изотопа того же элемента. Расчеты для случая, когда решетка состоит из нескольких элементов и содержит атомы их изотопов, более сложны. При этом для классического кристалла не должно наблюдаться каких-либо изменений, кроме изменения массы атома в том, узле, где находится изотоп. Однако в кристалле, свойства которого определяются квантовыми эффектами ( гелий - наиболее замечательный пример такого кристалла), можно ожидать искажений решетки и изменений эффективных значений постоянных связи в окрестности изотопического дефекта. [23]
Вследствие огромной относительной разницы в их атомных массах ( масса атома одного изотопа вдвое больше массы атома другого изотопа) свойства этих изотопов заметно различаются. Изотоп водорода с массовым числом 2 называют дейтерием и обозначают символом D. [24]
Вследствие огромной относительной разницы в их атомных массах ( масса атома одного изотопа вдвое больше массы атома другого изотопа) свойства этих изотопов заметно различаются. Изотоп водорода с массовым числом 2 называют дейтерием и обозначают символом D. [25]
Возможности экспериментального наблюдения резонанса на различных изотопах определяются их магнитными свойствами и естественным содержанием в смеси с другими изотопами. Искусственное приготовление изотопнозамещенных веществ ( кроме дейтерирован-ных ( для целей ЯМР-спектроскопии имеет весьма ограниченное значение. В табл. II-9 приведены свойства магнитных изотопов, играющих более важную роль в ЯМР-спектроскопии органических соединений. [26]
Если один изотоп адсорбируется первым и занимает наиболее активные центры, а затем на менее активных центрах адсорбируется другой изотоп и относительная активность различных центров после адсорбции не изменяется, то можно ожидать, что второй изотоп будет десорбироваться раньше, чем первый. Но если все центры с самого начала однородны или если после адсорбции происходит некоторое выравнивание, то должно наблюдаться смешение изотопов. Относящиеся сюда экспериментальные данные противоречивы. Так, Кейер и Рогинский [83] нашли, что никель и окись цинка не однородны по отношению к смесям водород - дейтерий, а Шуит [84] показал, что никелевый катализатор на силикагеле относительно этих же изотопов однороден. Эммет и Куммер [85] установили, что по отношению к окиси углерода половина поверхности железного катализатора синтеза аммиака однородна. Во всяком случае, может показаться, что этим методом скорее изучаются не врожденная гетерогенность поверхности, а подвижность адсорбата или возможность изменения прочности связи после адсорбции по механизму, подобному механизму индуцирования гетерогенности. Другой причиной такой гетерогенности является наличие ребер, вершин кристалликов и трещин в них; общепризнано, что эти центры могут давать значительный вклад в гетерогенность для физической адсорбции, при которой изменения энергии малы. [27]
Важнейшая особенность нестабильных изотопов - их радиоактивность, под которой понимают самопроизвольное превращение неустойчивого изотопа химического элемента в другой изотоп этого или другого элемента. Различают радиоактивность естественную и искусственную. Первая из них открыта А. Во многих случаях продукты радиоактивного распада сами оказываются радиоактивными, и тогда образованию стабильного изотопа предшествует цепочка из нескольких актов радиоактивного распада. Возможны разветвления радиоактивных превращений. [28]
Эти соотношения дают возможность вычислить количества отдельных изотопов радиоактивного ряда, находящиеся в радиоактивном равновесии с определенным количеством другого изотопа того же ряда, если известны их константы распада или периоды полураспада. Знание массовых количественных соотношений между отдельными изотопами радиоактивного ряда делает возможным в Ьшисление х и Т / г для одного изотопа, если значения их для другого изотопа известны. [29]
Эти соотношения дают возможность вычислить количества отдельных изотопов радиоактивного ряда, находящиеся в радиоактивном равновесии с определенным количеством другого изотопа того же ряда, если известны их константы распада или периоды полураспада. [30]
Страницы: 1 2 3