Разные изотоп
Cтраница 1
 |
Три изотопа углерода.| Некоторые распространенные изотопы. [1] |
Разные изотопы имеют разные массовые числа. Массовое число приблизительно равно массе изотопа. Итак, изотопы элемента имеют одинаковый атомный номер, но разные массовые числа. [2]
Разные изотопы имеют разное время жизни, так же как и биологические объекты, например бактерия, собака и галапагосская черепаха... Ученые могут определить скорость распада для каждого изотопа. [3]
Разные изотопы данного элемента имеют очень различную относительную распространенность, и в связи с этим различное влияние на атомный вес элемента. Насчитывается всего 272 стабильных и радиоактивных изотопов, весовое содержание которых не является пренебрежимо малым в природных условиях доступной исследованию части земного шара. Из числа радиоактивных нуклидов сюда относятся нуклиды, перечисленные в табл. 4.48 и 4.49. Остальные встречающиеся в природе радиоактивные нуклиды имеют значение лишь вследствие своей радиоактивности, а в весовом балансе элементов на Земле они не играют роли. [4]
Для разных изотопов одного элемента наблюдаются различия постулат, статистич. [5]
Атомы разных изотопов одного и того же элемента, отличаясь составом и свойствами ядра, имеют вместе с тем одинаковое строение электронной оболочки; поэтому химические свойства различных изотопов данного элемента почти тождественны. [6]
Ядра разных изотопов урана при действии нейтронов ведут себя различно: 238U, поглощая быстрые нейтроны, превращается в радиоактивный 239U с периодом полураспада в 23 мин, который затем, испуская нейтрон, превращается в новый искусственный элемент - нептуний 9aNp с периодом полураспада яз 24 дня. Далее нептуний, выбрасывая электрон, переходит в устойчивый элемент-плутоний Ри, период полураспада которого составляет 24 тыс. лет. [7]
Линии поглощения разных изотопов смещены в удаленные друг от друга части спектра. Одни из ядер поглощают в ультракоротковолновом диапазоне радиоволн, например ядра водорода и фтора; другие, например ядра изотопов бС и Р поглощают в коротковолновом диапазоне радиоволн, а ядра изотопов азота поглощают в средневолновом диапазоне в тех же условиях. Важно отметить, что область поглощения ядер одного и того же изотопа занимает промежуток спектра, который на несколько порядков меньше, чем интервал, отделяющий его от поглощения ядер другого изотопа. [8]
Диффузионное поведение разных изотопов одного и того же элемента в большинстве случаев различается мало ( изотопные эффекты малы), и поэтому обычно принимают, что диффузия радиоактивных атомов протекает с такой же скоростью, что и диффузия стабильных атомов исследуемого элемента. [9]
Непосредственное сравнение активности разных изотопов допустимо только при условии, что они изготовлены из одного и того же радиоактивного элемента или хотя бы имеют близкие энергии излучения при одинаковых схемах распада. В случае, когда пробеги бета-частиц в газе камеры меньше ее размеров и величина средней энергии бета-частиц известна, можно производить и абсолютные измерения. [10]
Периоды полураспада для разных изотопов могут быть самыми разными. [11]
Периоды полураспада для разных изотопов могут быть самыми разными. [12]
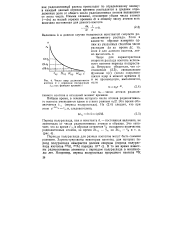 |
Число ядер радиоактивного и ее производную, выполняется. [13] |
Периоды полураспада для разных изотопов могут быть самыми разными. В то же время известны радиоактивные элементы с периодом полураспада в миллиарды лет. [14]
Для обозначения ядер разных изотопов и элементов принят способ написания, включающий обе основные характеристики - атомные номера и массовые числа. Около химического символа элемента вверху справа пишется индекс, обозначающий массовое число, а внизу слева ( или справа) - индекс, обозначающий атомный номер. [15]
Страницы: 1 2 3 4