Термодинамическая устойчивость - вещество
Cтраница 1
Термодинамическая устойчивость вещества является мерой возможности образования этого вещества или превращения его в другие вещества при определенных условиях, если система достигла равновесия. Кинетическая устойчивость вещества относится к скорости, с которой могут происходить превращения, ведущие к достижению равновесия. Проблемы кинетики будут обсуждены на стр. [1]
Эти реакции ограничивают термодинамическую устойчивость веществ в водном растворе. [2]
Расчет равновесных ( теоретических) выходов целевых и побочных продуктов реакции, определение термодинамической устойчивости веществ и направления само - и несамопроизвольного протекания реакций в изучаемых условиях является одним из важнейших этапов при исследовании новых химических реакций, при проектировании промышленных химических установок, при подборе оптимальных по составу катализаторов и разработке математических моделей для управления химическими процессами. Равновесный состав смеси химических веществ можно определить экспериментально или рассчитать по термическим данным с привлечением данных по теплоемкостям, теп-лотам и энтропиям веществ, а также по величинам изменения энергий Гельмгольца и Гиббса. [3]
Разрушение комплексного аниона при попытках удаления сольватирующего катион адденда нельзя объяснять только следствием применения повышенной температуры или высокого вакуума; существенно важно понижение термодинамической устойчивости вещества при его десольватации; повидимому, многие из подобных веществ могут быть термодинамически устойчивыми только в виде кристаллосольватов. [4]
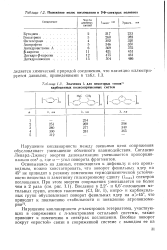 |
Положение полос поглощения в УФ-спектрах полиенов.| Значения А для некоторых типов31 карбоцепных полисопряженных систем. [5] |
Основываясь на данных, относящихся к дифенилу и его производным, можно констатировать, что поворот фенильных ядер на 45 не приводит к резкому изменению термодинамической устойчивости вещества и заметному гипсохромному сдвигу ( / - max) спектров поглощения. [6]
В свою очередь, вероятность определяется термодинамической устойчивостью веществ, последовательностью химических реакций, в ходе которых получено данное чистое вещество, различными стадиями очистки. [7]
Стандартные энтропии алканов показывают, что неразветвленный изомер обычно характеризуется более высоким значением, чем разветвленные изомеры, из-за сферических препятствий в последних, снижающих число внутренних вращательных энергетических состояний. Так, октан и его изомеры - 3-этилгексан, 2 2-диметилгексан и 2 2 3 3-тетраметилбутан - имеют энтропию 111, 109 5, 103 и 94 энтр. Наличие двойной связи в алкене ненамного снижает стандартную энтропию по сравнению с энтропией алкана, особенно если двойная связь в первом является концевой, но циклизация вызывает существенное снижение энтропии, и для соединений пентан, пен-тен-1 и циклопентан значения этой величины равны 83 3, 83 1 и 70 энтр. Вариации энтропии, которые зависят от размера цепи, в большой степени определяют термодинамическую устойчивость веществ. Так, сравнительная легкость, с которой может быть проведен пиролиз нефти ( стр. [8]
Стандартные энтропии алканов показывают, что неразветвленный изомер обычно характеризуется более высоким значением, чем разветвленные изомеры, из-за стерических препятствий в последних, снижающих число внутренних вращательных энергетических состояний. Так, октан и его изомеры - 3-этилгексан, 2 2-диметилгексан и 2 2 3 3-тетраметилбутан - имеют энтропию 111, 109 5, 103 и 94 энтр. Наличие двойной связи в алкене ненамного снижает стандартную энтропию по сравнению с энтропией алкана, особенно если двойная связь в первом является концевой, но циклизация вызывает существенное снижание энтропии, и для соединений пентан, пен-тен-1 и циклопентан значения этой величины равны 83 3, 83 1 и 70 энтр. Вариации энтропии, которые зависят от размера цепи, в большой степени определяют термодинамическую устойчивость веществ. Так, сравнительная легкость, с которой может быть проведен пиролиз нефти ( стр. А / / / увеличивается почти аддитивно с вводом каждой СН2 - грушш в алкильную цепь. [9]
Страницы: 1