Изучение - диаграмма
Cтраница 1
Изучение диаграммы позволяет сделать следующие заключения. [1]
Изучение диаграммы состав - свойство имеет большое значение для синтеза новых соединений. На основе полученной диаграммы можно сознательно выбрать условия образования и выделения соответствующего вещества. [2]
Изучение диаграммы состав - свойство приводит к геометрической характеристике основного химического закона кратных пропорций. Мы имеем право говорить об общем геометрическом методе изучения химических превращений. [3]
Изучение диаграмм Венна подсказало автору некоторые изменения решения проблемы разрешения для исчисления одноместных предикатов. Венн не занимался проблемами разрешимости и разрешения. Но для того, чтобы обосновать его метод преобразования информации ( в которую могут входить и частные предложения), нами решается проблема разрешения для формул исчисления одноместных предикатов с помощью только диаграмм Венна. Из ее решения получается общее правило, позволяющее обозревать логические следствия данных посылок. [4]
Изучение диаграммы позволяет сделать вывод, что такие конструкции, как переменная, константа без знака, имя функции являются выражениями. Из диаграммы также следует, что более простые конструкции, имеющие даже свои названия ( множитель, слагаемое), являются составляющими более сложных конструкций. [5]
Изучение диаграммы состав-свойство приводит к геометрической характеристике основного химического закона кратных пропорций. [6]
Изучение диаграммы состав - свойство приводит к геометрической характеристике основного химического закона кратных пропорций. Мы имеем право говорить об общем геометрическом методе изучения химических превращений. [7]
Изучение диаграммы состав-свойство приводит к геометрической характеристике основного химического закона кратных пропорций. [8]
Изучение диаграмм давление пара - состав показывает, что компоненты раствора ведут себя не так, как это следовало бы ожидать на основании теоретических предпосылок. [9]
Изучение диаграмм состав-температура плавления, диаграмм плавкости, или термический анализ, было введено Н. С. Курнаковым в практику работы еще в 1899 г. [ 4, II, стр. Диаграммы плавкости являются частным случаем ( р - const) более общей диаграммы t - р-с. В данном случае свойство - температура фазового превращения является одновременно и фактором равновесия. [10]
 |
Температура плавления системы LiCl - КС1. [11] |
Изучение диаграмм плавкости является одним из методов физико-химического анализа, разработанного Н. С. К у р н а к о-в ы м и его школой. [12]
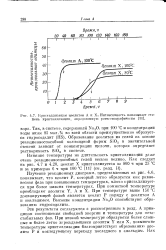 |
Кристаллизация цеолитов А и X. Интенсивность показывает степень кристаллизации, определенную рентгенографически. [13] |
Изучение реакционных диаграмм, представленных на рис. 4.6, показывает, что цеолит Р, который легко образуется как равновесная фаза при повышенных температурах, плохо кристаллизуется при более низких температурах. При комнатной температуре преобладают цеолиты Y, А и X. При температуре выше 150 С доминирующей фазой является цеолит Р наряду с цеолитом А и анальцимом. Высокие концентрации Na20 способствуют образованию гидросодалита. [14]
Изучение диаграммы плавкости свинца с различными присадками позволяет сформулировать следующую теорию механизма действия этих добавок на свойства сплавов. Добавки, плохо или незначительно растворяющиеся в свинце, как, например, Sb, Cd, Sn, Си, Те, Са, Mg, при охлаждении сплава выделяются в коллоидном состоянии, располагаясь по границам зерен свинца, и поэтому механически препятствуют росту зерен. [15]
Страницы: 1 2 3 4