Изучение - диаграмма - равновесие
Cтраница 1
Изучение диаграмм равновесия и физических свойств некоторых систем, включающих переходные металлы первого длинного периода таблицы Менделеева, показало, что валентность переходных металлов может изменяться не только в различных системах, но и в пределах одной системы при изменении состава сплавов. [1]
Изучение диаграммы равновесия системы Na2O - PbO - SiO2 дало возможность указать область трудно кристаллизующихся стекол. На диаграмме, эта область очерчена пунктиром. [2]
Построение и изучение диаграмм равновесия составляет предмет термического или, как его часто теперь называют, физико-химического анализа. Применение его к металлическим сплавам лежит в основе металлографии. [3]
На основе изучения диаграмм равновесия реакций СО и Н - г с закисью железа ( FeO) установлено максимально допустимое содержание кислорода в пламени при сварке стали, отвечающее ( 30 1 3, при котором окисления сварочной ванны еще не происходит. [4]
На основе изучения диаграмм равновесия реакций СО и Н - г с закисью железа ( FeO) установлено максимально допустимое содержание кислорода в пламени при сварке стали, отвечающее 50 1 3, при котором окисления сварочной ванны еще не происходит. [5]
Успех метода спекания для работ по изучению диаграмм равновесия в большой степени зависит от возможности удаления этих примесей при высокой температуре в вакууме или водороде. [6]
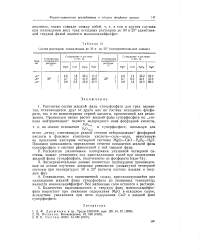 |
Состав растворов, охлажденных до 50 и до 25 ( экспериментальные данные. [7] |
Экспериментальные данные полностью подтвердили произведенные на основе изучения диаграмм равновесия упомянутой четверной системы при температурах 50 и 25 расчеты состава жидких и твердых фаз. [8]
Политермический фазовый метод был применен нами для быстрого определения температур фазовых равновесий некоторых промышленных стекол, а также для ориентировочного изучения диаграмм равновесия ряда систем. [9]
Диаграммы равновесия позволяют, таким образом, наметить возможные варианты разложения редкоземельных титанониобиевых концентратов серной кислотой и установить условия проведения процесса. С помощью серной кислоты лопаритопый, перонскитовый, сфеновый и другие концентраты могут быть переведены в продукты, которые пригодны для дальнейшего разделения и получения полезных компонентов в чистом виде. Этими продуктами являются сульфаты или двойные сульфаты с титаном. Опыты по разложению концентратов серной кислотой полностью подтверждают выводы, сделанные на основе изучения диаграмм равновесия. [10]
Если двухфазный сплав состоит из смеси соприкасающихся друг с другом кристаллов фаз Л и В, то поверхностная энергия, связанная с поверхностью раздела А-В обычно зависит от относительной ориентировки кристаллов названных фаз. В этом случае для истинного равновесия необходимо, чтобы кристалл А соприкасался с кристаллом В по поверхности с наиболее низкой поверхностной энергией. Величина этой энергии часто имеет важное значение для объяснения мелкокристаллической структуры сплавов. Например, известно, что в случае равновесия между твердой фазой и жидкостью растворимость твердой фазы возрастает с уменьшением размеров частицы. Аналогичное явление также наблюдается при взаимодействии между твердыми фазами. Почти во всех работах по изучению диаграмм равновесия влияние поверхностной энергии во внимание не принимается, так как при размерах кристаллов больше 0 010 мм эта энергия относительно мала. [11]
Страницы: 1