Изучение - диаграмма - состояние - система
Cтраница 1
Изучение диаграмм состояния систем K3SO4 - - V2O6 и K2S2O7 - V2O6 показало, что эти системы имеют значение как модели при изучении состояния активного компонента ванадиевых катализаторов, широко применяющихся для окислительных процессов, в частности в сернокислотной промышленности. [1]
Изучение диаграммы состояния системы NaF - A1F3 - LiF с применением дифференциально-термического, рентгенографического и кристаллооптического методов анализа показало, что систем-а характеризуется одиннадцатью полями первичной кристаллизации и одиннадцатью нонвариантными процессами. Определены границы полей первичной кристаллизации NaAlF4, LiAlF4, Ы5А1зРм, NaaLisAbF, Na5Li5Al6F28 и уточнены границы полей кристаллизации других соединений. Соединение Na2LiAlF6 не кристаллизуется первично. [2]
Изучение диаграммы состояния системы LiF - - A1F3, выполненное с применением дифференциально-термического, рентгенографического и кристаллооптического анализов, показало, что в ней образуются три соединения: ранее известный литиевый криолит ( Li3AlF6), литиевый хиолит ( 1л5А1зРн) и фторалюминат лития ( LiAlFO. В системе дополнительно обнаружены эвтектическая и перитектическая точки. [3]
Изучение диаграмм состояния двойных фторидных систем [5-7] показало, что диаграммы состояния систем LiF - BeF2 и ZnO - SiO2 ( рис. 104), CaF2 - BeF2 и ZrO2 - SiO2, MgF2 - BeF2 и TiO2 - SiO2 очень похожи. Вместо этого кривая ликвидуса в области, богатой BeF2, идет относительно полого, что указывает на некоторую склонность к расслаиванию. В силикатных системах, содержащих щелочноземельные элементы, протяженность области расслаивания уменьшается при увеличении размера катиона-модификатора. [4]
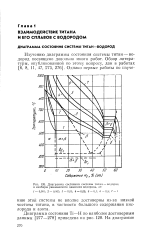 |
Диаграмма состояния системы титан - водород и изобары равновесного давления водорода, ат. [5] |
Изучению диаграммы состояния системы титан - водород посвящено довольно много работ. [6]
При изучении диаграммы состояния системы FeO - Si02 встречались необычные трудности из-за того, что закись железа очень легко распадается на металлическое железо - - окись железа. [7]
Данное исследование сплавов и изучение диаграммы состояния системы цирконий - ниобий - алюминий было выполнено в 1956 г. В литературе до настоящего времени нет указания на изучение данной диаграммы. [8]
Излагаются экспериментальные результаты по изучению диаграммы состояния системы Zr-Си - Мо и некоторых физико-химических свойств тройных сплавов, богатых цирконием. Установлена широкая область тройного ( ( - твердого раствора при 1000 С. Построена проекция диаграммы на плоскосгь концентрационного треугольника, написана схема реакций. [9]
Излагаются результаты экспериментального исследования по изучению диаграммы состояния системы Zr - V - Nb методами физико-химического анализа по трем лучевым разрезам, секущим циркониевый угол диаграммы с отношением V: Nb4: 1, 1: 1, 1: 4, и одному лучу соединяющему ниобиевый угол диаграммы и химическое соединение ZrV2 в интервале концентраций от 1 до 95 % V Nb при температурах 1000, 700 и 500 С. Установлено, что твердый раствор на основе р-циркония при 1000 С распадается на два твердых раствора: р и PNh Y Область расслоения с понижением температуры до 700 С расширяется, постепенно переходя в двойную систему цирконий - ниобий. Построена проекция диаграммы состояния на концентрационный треугольник и написана схема реакций. [10]
В таком виде оно широко применяется при изучении диаграмм состояния систем, образованных практически нелетучими веществами. При этом давление пара настолько мало, что им пренебрегают. Подобные системы называются конденсированными. При изучении изотерм растворимости ( растворимость солей при постоянной температуре) правило фаз имеет такое же написание. [11]
Описанные выше примеры касались использования направленной кристаллизации при изучении диаграмм состояния эвтектических и перитектических систем. Отметим, что возможности рассматриваемого метода на этом не ограничиваются. Однако соответствующие экспериментальные исследования не опубликованы. [12]
Большой интерес для оценки необходимой степени осушки хлора применительно к производству жидкого хлора представляют данные14, приведенные на конференции электрохимического общества США в 1966 г. При изучении диаграммы состояния системы С12 - Н2 было установлено, что в состоянии равновесия содержание воды в газообразном хлоре при 40 - 60 С в 4 раза больше, чем в жидком хлоре. [13]
 |
Типичные марки хромистой нержавеющей стали. [14] |
Марка 1X13, содержащая малое количество углерода, представляет пример стали, называемой часто нержавеющим железом. Изучение диаграмм состояний системы Fe - С - Сг показывает, что при составах, отвечающих этой марке, наряду с хромистым ферритом могут получаться аустенит и продукты его распадения. [15]
Страницы: 1 2