Изучение - кинетическая закономерность
Cтраница 1
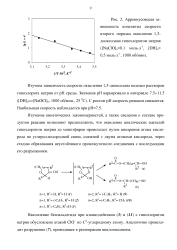 |
Аррениусовская зависимость константы скорости второго порядка окисления 1 3-диоксолана гипохлоритом натрия ( [ NaClO ] моль-л 1, [ DH ] 0 моль-л 1, 1000 об / мин. [1] |
Изучение кинетических закономерностей, а также сведения о составе продуктов реакции позволяют предположить, что окисление циклических ацеталей гипохлоритом натрия до моноэфиров происходит путем внедрения атома кислорода по углерод-водородной связи, смежной с двумя атомами кислорода, через стадию образования неустойчивого промежуточного соединения с последующим его разрушением. [2]
Изучение кинетических закономерностей и влияния структуры соединений в этой реакции206 209 привели к выводу, что первой стадией процесса является оксиметаллирование. Ввиду склонности первичных аддуктов к распаду выделить эти аддукты и доказать их строение удалось только в случае окситаллирования норборнена и нор-борнадиена 72 21, где стабильность продуктов присоединения повышена, вероятно, за счет внутримолекулярной координации таллий - кислород. [3]
Изучение кинетических закономерностей и механизма полимеризации этилена в присутствии триаллилхрома и тетра - / шс-я-аллил-циркония [938, 939] привело к выводу о том, что катализаторами полимеризации являются не сами я-аллильные соединения, а продукты их взаимодействия с водой, неизбежно присутствующей в реакционной среде. [4]
Изучение кинетических закономерностей включает следующие этапы: экспериментальное исследование зависимости скорости реакции от условий проведения процесса; обоснование механизма процесса на основании полученных экспериментальных данных и вывод аналитических зависимостей скорости процесса от внешних условий на основании экспериментальных данных и принятого механизма процесса; обоснование выведенной зависимости путем специально поставленных экспериментов. [5]
Изучение кинетических закономерностей эпоксидирования 1 2-эпоксиоктена - 7 еще раз подтвердило, что независимо от природы олефика реакция имеет первый порядок по гидропероксиду и катализатору. [6]
Изучение кинетических закономерностей взаимодействия кислорода и серебра показало, что скорость поглощения кислорода почти не зависит от его парциального давления и равна 7 - Ю12 атомов в 1 см2 в секунду при полном покрытии серебра кислородом. Энергия активации равна 147 кДж / моль ( 35 ккал / моль), предэкспоненциальный множитель уравнения Аррениуса равен 3 7 - 1027 атомов в 1 см2 в секунду. [7]
Изучение кинетических закономерностей превращения топлива в дизеле крайне осложняется гетерогенным характером его смеси с воздухом. Поэтому исследование самовоспламенения ограничивается обычно анализом зависимости его задержек от давления и температуры. Эта зависимость выражается эмпирическим уравнением [ 43, стр. [8]
Изучение кинетических закономерностей распада полимера с 1 2 4-оксадиазольным циклом позволило установить, что процесс термодеструкции начинается с разрушения гетероцикла. При этом прежде всего происходит радикальный разрыв О - N - и О - С-связей. Разрыв О - N-связи приводит к выделению азота, окислов углерода и дициана, разрушение связи О - С - к выделению кислорода и динитрилов кислот, из которых были получены полиоксадиазолы. [9]
Изучение кинетических закономерностей распада полимера с 1 2 4-оксадиазольным циклом позволило установить, что процесс термодеструкции начинается с разрушения гетероцикла. При этом прежде всего происходит радикальный разрыв О-N - и О-С - связей. Разрыв О-N - связи приводит к выделению азота, окислов углерода идициана, разрушение связи О-С - к выделению кислорода и динитрилов кислот, из которых были получены полиоксадиазолы. [10]
Изучение кинетических закономерностей процессов полимеризации проводят в атмосфере инертных газов, тщательно очищенных от кислорода и влаги. [11]
Изучение кинетических закономерностей полимеризации метилметакрилата [ 109, ПО ] и стирола [110] под воздействием у-излучения при 20 - 100 в присутствии окиси магния, являющейся - полупроводником [111], показало, что выход полимеров Находится в линейной зависимости от величины / Y2 где / - мощность дозы излучения. Как известно, такая зависимость характерна для обрыва кинетических цепей за счет рекомбинации растущих макрорадикалов и свидетельствует о радикальном механизме полимеризации. В аналогичных условиях на поверхности окиси цинка, являющейся я-полупроводником, метилметакрилат не полимеризуется что, очевидно, связано с тем, что образующиеся ион-радикалы О - легко захватывают свободные электроны, концентрация которых в окиси цинка довольно высока, и дезактивируются, гае успев прореагировать с мономером. [12]
Изучение кинетических закономерностей полимеризации этилена на системе ( CsHsbTiCb-Al HsbCl в среде хлористого этила показало, что, несмотря на гомогенный характер катализатора, концентрация центров роста в растворе сравнительно низка и составляет лишь малую долю от общей концентрации соединений титана. [13]
 |
Значения констант скоростей реакций и их энергий активации. [14] |
Изучение кинетических закономерностей каталитического присоединения спиртов осложняется параллельно протекающей реакцией изомеризации: аллена метилацетилен. [15]
Страницы: 1 2 3 4