Адсорбция - анион
Cтраница 3
Для исследования адсорбции анионов нами были сняты, кроме С-ф-кривых, также и 0-ф-кривые на капиллярном электрометре Гун. [31]
В случае адсорбции анионов на положительно заряженной поверхности подобный скачок потенциала оказывается направленным в противоположную сторону по сравнению со скачком потенциала в двойном ионном слое. Суммарная разность потенциалов между металлом и раствором уменьшается. Для ее компенсации количество зарядов в двойном ионном слое должно быть увеличено. В сочетании с утечкой заряда из ионной обкладки двойного слоя к металлу это приводит к заметному увеличению емкости электрода. [32]
Исследование процессов адсорбции анионов при помощи меченого хлора ( С1Е6, удельная активность 0 058 мкюри / г) на электродах из прессованного-хрома по изменению активности электролита позволило получить результаты, которые подтвердили высказанную выше точку зрения. [33]
Объясняется это адсорбцией аниона соли и катиона основания с образованием основных солей, присутствующих в небольших количествах в прокаленном препарате. [34]
 |
Кривые / 4 - ф в 0 01 М рас. [35] |
Снижение фототока при адсорбции анионов связано прежде всего с влиянием г) - потенциала на фотоэмиссию, и если бы влияние анионов сводилось лишь к этому, то по соответствующему сдвигу кривых фототока можно было бы определить изменение г з - потенциала при адсорбции и рассчитать таким образом потенциал во внешней плоскости Гельмгольца. [36]
Таким образом, адсорбция анионов, сдвигающая т в отрицательную сторону, несколько тормозит разряд, в то время как катионы оказывают противоположное действие. Однако количественно в своей простейшей форме этот поправочный член не может полностью объяснить изменения на поверхности, покрытой кислородом. Более того, реагирующие вещества ( анионы) могут адсорбироваться на поверхности при высоких потенциалах так, что их поверхностная концентрация может не влиять заметно или влиять совсем иначе на - эффект. [37]
Получены данные по адсорбции аниона СН3СОО - на моно - и ди-карбоксилцеллюлозах с различным содержанием СООН-групп. [38]
 |
Зависимость адсорбции катионов Na ( /, 1 и анионов 5ОГ2 ( 2, 2 на Pt / Pt-электроде в растворе 10 - 3 н. H2SO4 3 - 10 - 3 н. Na2SO4. [39] |
В присутствии метанола адсорбция анионов SOj снижается в широком интервале потенциалов. После окисления адсорбированного метанола она достигает того же значения, которое наблюдалось в отсутствие метанола. Адсорбция катионов Na возрастает при адсорбции метанола. [40]
Указываются следующие причины адсорбции анионов и анионного обмена. [41]
 |
Зависимость Де горбов от lg ( aHa c /. [42] |
Поэтому влияние характера адсорбции аниона на сдвиг горбов также не вызывает сомнения. [43]
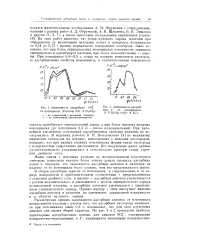 |
Зависимость адсорбции 80 от потенциала. ( Раствор 0 01 N ll SOt.| Зависимость адсорб. [44] |
Рассмотрение кривых зависимости адсорбции анионов от потенциала неокисленной платины с учетом того, что адсорбция кислорода начинается при потенциалах выше 0 4 в, показывает, что для всех изученных анионов они имеют общий характер. [45]
Страницы: 1 2 3 4