Адсорбция - иод
Cтраница 2
Имеются данные43 об адсорбции иода различными минеральными адсорбентами. [16]
Возможно, что адсорбция иода на адсорбированных окислах иода происходит лучше, чем на ТП, или что эти окислы улетучиваются немедленно после образования, оставляя чистую поверхность ТП. Результат существенно не изменяется, если сначала впустить кислород, а затем, откачав его, пустить иод. [17]
В Советском Союзе адсорбция иода активированным углем и все предшествующие ей операции осуществляются в виде поточного процесса. За рубежом имеются установки, где адсорбция оформлена в виде периодического процесса. Последние стадии получения иода - отмывка угля и выделение иода из концентратов - всюду осуществляются периодически. [18]
Имеются данные43 об адсорбции иода различными минеральными адсорбентами. [19]
Например, величина адсорбции иода, имеющего относительно небольшие размеры молекул, практически одинакова на крупнопористом древесном угле и мелкопористом плотном угле, тогда как величина адсорбции красителя ( ме-тиленовый голубой), состоящего из больших молекул, на мелкопористом угле в четыре раза меньше, чем на крупнопористом. Это указывает на то, что по мере увеличения размеров частиц адсорбтива число пор адсорбента, которые остаются еще доступными для этих частиц, уменьшается. [20]
Менее убедительные доказательства адсорбции иода были получены по измерениям фарадеевского импеданса [14-16], причем следует подчеркнуть, что во многих случаях адсорбционная емкость не была обнаружена совсем. [21]
Одним из источников ошибок является адсорбция иода на поверхности иодида меди. Адсорбированный иод придает осадку темно-желтую окраску и тем самым не позволяет получить отчетливую конечную точку. [22]
Активированный уголь, применяемый для адсорбции иода. [23]
Исходя из того, что адсорбция иода и родамина С из воды значительно больше, чем из н-пропанола, можно ожидать, что, поместив образец ПЭТФ, достигший адсорбционного равновесия в воде, в чистый к-пропанол, можно будет наблюдать процесс десорбции в том случае, если адсорбированное вещество не прореагировало химически с поверхностью адсорбента. Было обнаружено, что как иод, так и родамин С показывают значительную десорбцию при замене воды на н-пропанол, что свидетельствует о физическом характере адсорбции. Процесс десорбции иллюстрируют данные рис. 4.6, на котором представлены зависимости относительного количества десорбированного вещества в w - пропаноле к общему количеству адсорбированного вещества из воды от степени вытяжки ПЭТФ. Как видно из рисунка, в области относительно малых значений деформации вследствие десорбции адсорбент теряет 85 - 95 % сорбтива. Однако, как для родамина С, так и для иода, десорбция резко уменьшается при увеличении степени вытяжки. Очевидно, что процесс десорбции также чрезвычайно чувствителен к структуре полимера и может быть использован как метод ее исследования. [24]
Активированный уголь, применяемый для адсорбции иода. [25]
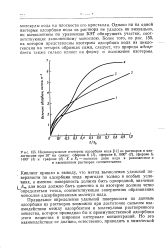 |
Индивидуальные изотермы адсорбции иода из растворов в цик. [26] |
Однако ни на одной изотерме адсорбции иода из раствора не удалось ни визуально, ни вычислением по уравнению БЭТ обнаружить участки, соответствующие заполненному монослою. Более того, из рис. 155, на котором представлены изотермы адсорбции иода из цикло-гексана на четырех образцах сажи, следует, что природа адсорбента также сильно влияет на форму и положение изотермы. [27]
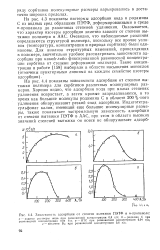 |
Зависимость адсорбции от степени вытяжки ПЭТФ в н-пропаноле. [28] |
На рис. 4.3 показаны изотермы адсорбции иода и родамина С из водных сред образцами ПЭТФ, деформированными в среде н-пропанола до различных степеней удлинения. Оказывается, что характер изотерм адсорбции заметно зависит от степени вытяжки полимера в ААС. Очевидно, что наблюдаемые различия определяются структурой полимера, поскольку все прочие условия ( температура, концентрация и природа сорбтива) были одинаковы. Для анализа структурных изменений, происходящих в полимере, значительно удобнее рассматривать зависимости адсорбции при какой-либо фиксированной равновесной концентрации сорбтива от степени деформации полимера. [29]
Райерсон и Камерон измерили также адсорбцию иода на силикагеле. Эти результаты удивительны, так как были получены очень малые значения адсорбции. Пользуясь значением поверхности, полученным из изотерм адсорбции брома, и предполагая, что упаковка молекул иода на поверхности та же, что и в жидком состоянии, находим vm равным 2 93 миллимоля иода на грамм силикагеля. Это указывает на то, что силы адсорбции значительно слабее, чем силы, действующие между молекулами иода в жидком состоянии. [30]
Страницы: 1 2 3 4