Адсорбция - катализатор
Cтраница 1
Адсорбция катализатора в целом зависит от адсорбции его основной и кислотной форм, находящихся в протолитическом равновесии. Батлера, полученным для органических оснований в нейтральных и кислых растворах [281, 292], значительно выше, чем кислотной. [1]
Считая, что адсорбция катализатора подчиняется изотерме Генри, и принимая во внимание уравнения ( 42) и ( 112) ( см. стр. [2]
Спад тока вызван падением адсорбции катализатора при сдвиге потенциала в отрицательную сторону, но потенциал максимума не совпадает с потенциалом максимальной адсорбции. Уравнения (71.8) и (71.10) количественно описывают волны каталитического выделения водорода в буферных растворах в присутствии хинина ( рис. 200) и некоторых других органических оснований. [3]
Спад тока вызывается снижением адсорбции катализатора при сдвиге потенциала в отрицательную сторону. [4]
При этом, очевидно, адсорбция катализатора перестает подчиняться уравнению ( 111) и подчиняется уже выражению ( 110) или даже ( 112) ( см. стр. [5]
Однако в соотношении (7.78) V np / d, а индексом о обозначены гипотетические токи, которые наблюдались бы в условиях независимости адсорбции катализатора от потенциала электрода и ее равенства величине, реализующейся при потенциале максимальной адсорбции Ет. На практике такие условия не выполняются, а величины / и / пр можно связать с реально измеряемыми каталитическими токами, если учесть изменение степени заполнения поверхности электрода органическим веществом в с отклонением потенциала от значения Ет. [6]
Майрановский объясняет протеканием тех же процессов, о которых говорилось выше. Однако благодаря адсорбции катализатора в этом случае химическая реакция протонизации происходит на самой электродной поверхности. Часто наблюдаются также смешанные токи [84 - 87], когда предшествующая реакция ( XI) протекает и на поверхности электрода и в объеме раствора. Адсорбция катализатора в целом зависит от адсорбции его кислотной и основной форм, находящихся между собой в протолитическом равновесии. Поверхностная активность основной формы значительно превосходит активность кислотной формы; более того, адсорбируемость кислотной ( катионной) формы катализатора на отрицательно заряженной поверхности электрода изменяется с потенциалом гораздо меньше, чем основной, поэтому изменение адсорбируемости катализатора в целом определяется в основном изменением адсорбируемости его основной формы. [7]
Майрановский объясняет протеканием тех же процессов, о которых говорилось выше. Однако благодаря адсорбции катализатора в этом случае химическая реакция протонизации происходит на самой электродной поверхности. Часто наблюдаются также смешанные токи [84 - 87], когда предшествующая реакция ( XI) протекает и на поверхности электрода и в объеме раствора. Адсорбция катализатора в целом зависит от адсорбции его кислотной и основной форм, находящихся между собой в протолитическом равновесии. Поверхностная активность основной формы значительно превосходит активность кислотной формы; более того, адсорбируемость кислотной ( катионной) формы катализатора на отрицательно заряженной поверхности электрода изменяется с потенциалом гораздо меньше, чем основной, поэтому изменение адсорбируемое катализатора в целом определяется в основном изменением адсорбируемости его основной формы. [8]
Выход полимера при наличии НС1 в растворе катализатора при отношении НС1: А1С13 до 0 2 или в шихте до 0 8 не изменяется, но при увеличении значений указанных отношений снижается. Понижение выхода в этом случае, вероятно, связано с адсорбцией катализатора агломерированными частицами полимера. [9]
Малая величина емкостного тока позволяет работать со стационарным ртутным электродом при максимальной чувствительности полярографа. Высокая чувствительность определения достигается при этом также за счет накопления катализатора на поверхности электрода при выдерживании его под током в течение некоторого строго контролируемого времени, поскольку наблюдаемые каталитические волны являются поверхностными и адсорбция катализатора на поверхности электрода определяет высоту волны. [10]
Величина адсорбции кислоты была примерно такой же, как и в первом случае, но равновесные концентрации были на порядок выше - 0 5 - 0 6 N. Особенно резко это сказалось при увеличении объемной скорости до 13 5 мл / мл-ч, где для прокаленного после адсорбции катализатора каталитическая активность снизилась на 85 % от исходной. Следовательно, в соответствующих кинетических условиях оценки каталитической активности и для катализатора Гудри может быть также обнаружено отравляющее действие фосфорной кислоты. [11]
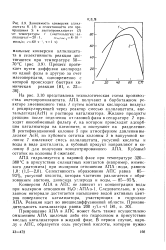 |
Зависимость конверсии аллил-ацетата К ( / и селективности его превращения S в ацетопропилацетат ( 2 от температуры / ( ацетальдегид. ал-лилацетат 20. 1, Cco ( oAo2 8 - 10 (. [12] |
На рис. ЗЛО представлена технологическая схема производства ацетопропилацетата. АПА получают в барботажном реакторе змеевикового типа / путем контакта кислорода воздухл с рециркулирующей через реактор смесью аллилацетата, аце-тальдегида ( АсН) и раствора катализатора. Жидкие продукты реакции после отделения от газовой фазы в сепараторе 2 проходят ионообменный фильтр 4, на котором происходит адсорбция катализатора на катионите, и поступают на разделение, В ректификационной колонне 5 при атмосферном давлении выделяют АсН, из кубового остатка колонны 5 в вакуумной колонне 7 извлекают смесь аллилацетата, уксусной кислоты и воды в виде дистиллята, а кубовый продукт направляют в колонну 8 для получения концентрированного АПА. Кубовый остаток из колонны 8 сжигают. [13]
Майрановский объясняет протеканием тех же процессов, о которых говорилось выше. Однако благодаря адсорбции катализатора в этом случае химическая реакция протонизации происходит на самой электродной поверхности. Часто наблюдаются также смешанные токи [84 - 87], когда предшествующая реакция ( XI) протекает и на поверхности электрода и в объеме раствора. Адсорбция катализатора в целом зависит от адсорбции его кислотной и основной форм, находящихся между собой в протолитическом равновесии. Поверхностная активность основной формы значительно превосходит активность кислотной формы; более того, адсорбируемость кислотной ( катионной) формы катализатора на отрицательно заряженной поверхности электрода изменяется с потенциалом гораздо меньше, чем основной, поэтому изменение адсорбируемости катализатора в целом определяется в основном изменением адсорбируемости его основной формы. [14]
Майрановский объясняет протеканием тех же процессов, о которых говорилось выше. Однако благодаря адсорбции катализатора в этом случае химическая реакция протонизации происходит на самой электродной поверхности. Часто наблюдаются также смешанные токи [84 - 87], когда предшествующая реакция ( XI) протекает и на поверхности электрода и в объеме раствора. Адсорбция катализатора в целом зависит от адсорбции его кислотной и основной форм, находящихся между собой в протолитическом равновесии. Поверхностная активность основной формы значительно превосходит активность кислотной формы; более того, адсорбируемость кислотной ( катионной) формы катализатора на отрицательно заряженной поверхности электрода изменяется с потенциалом гораздо меньше, чем основной, поэтому изменение адсорбируемое катализатора в целом определяется в основном изменением адсорбируемости его основной формы. [15]
Страницы: 1