Изучение - кинетика - восстановление
Cтраница 1
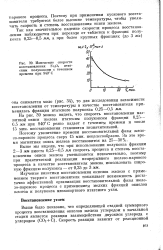 |
Изменение скорости восстановления Fe3O4 итат-ским полукоксом с течением времени при 940 С. [1] |
Изучение кинетики восстановления окислов железа с применением твердого восстановителя показывает возможность достаточно эффективной организации восстановительной фазы железо-парового процесса с применением мелких фракций окислов железа и полукокса низкосортного итатского угля. [2]
Изучение кинетики восстановления окислов железа и окис-ных смешанных контактов газовыми и твердыми восстановителями ( разные виды топлива) показало, что реакции восстановления контактов протекают с большими скоростями, чем реакции восстановления окислов железа. [3]
Изучение кинетики восстановления редкоземельных окислов углеродом позволило Ашару предложить метод разделения окислов РЗЭ. [4]
При изучении кинетики восстановления механических смесей окиси свинца с кварцем обнаружено затормаживание процесса, вызываемое образованием силикатов свинца. Установлено, что процесс восстановления интенсифицирует силикатообразование. [5]
Опыты по изучению кинетики восстановления окислов металлов углеродом были проведены в условиях наибольшего контакта окислов и углерода ( прессованные шарики) при атмосферном давлении. Скорость реакции определялась по изменению веса шарика торзионными весами, которое автоматически записывалось на фотопленку. [6]
Проведенное ранее [1-7] изучение кинетики восстановления нитробензола, нитрозобензола, фенилгидроксиламина и некоторых производных нитробензола в различных физико-химических условиях, с одновременным исследованием потенциала катализатора в ходе реакции, позволило сделать вывод о том, что механизм каталитического восстановления ароматических нитросоединений зависит от относительной адсорбции водорода и восстанавливаемого соединения на поверхности катализатора. [7]
Эти работы посвящены изучению кинетики восстановления высокодисперсных окислов металлов метаном. [8]
Рассмотренные выше работы по изучению кинетики восстановления окислов металлов углеродом показывают, что в выводах различных авторов имеются противоречивые суждения о кинетике процесса и его определяющей стадии. [9]
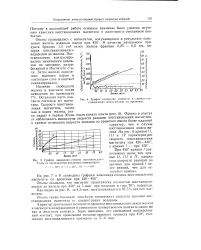 |
График изменения скорости и степени восстановления окиси железа со временем.| График изменения степени восстановления РеоОз со временем при различных температурах. [10] |
Поэтому в дальнейшей работе основное внимание было уделено изучению кинетики восстановления магнетита в железном и смешанном контактах. [11]
 |
Расход водорода при восстановлении. [12] |
Авторы, с нашей точки зрения, методически правильно и тщательно провели изучение кинетики низкотемпературного восстановления окислов железа и руд водородом. Методика, использованная ими, давала возможность снимать кинетическую кривую восстановления РезОз с отсчетом через 1 мин. Режим процесса, по мнению авторов, был выбран применительно к кинетической области. Кинетическая область наблюдалась при достаточно большой скорости циркуляции газа - 2400 см. / мин. Использование циркуляционной системы является методически правильным решением вопроса работы с большими скоростями газа-восстановителя. [13]
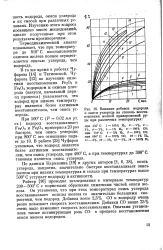 |
Влияние добавок водорода к окиси углерода на степень восстановления мелкой криворожской руды при различных температурах. [14] |
В то же время в работах Чу-фарова [14] и Татиевской, Чу-фарова [12] по изучению кинетики восстановления Рв20з и Fes04 водородом и окисью углерода ( вакуум, начальный период процесса) указывается, что водород при низких температурах является более активным восстановителем, чем окись углерода. [15]
Страницы: 1 2