Адсорбция - микропримесь
Cтраница 2
Поскольку из абсолютных изотерм в области Генри может быть получено значение константы адсорбционного равновесия, по изменению константы можно судить об изменении химических свойств поверхности и п характере взаимодействия микропримеси с поверхностью адсорбента. Выло установлено, что для адсорбции микропримеси триэтоксифосфина из триэтоксисиланн SiH ( OC2ns) 3 значения абсолютных емкостей для гидро-ксилированного и дегидроксилирован-ного силикагелей отличались почти п 2 раза ( 47 ], в то время как адсорбция РеСЬ из SiCU на этих же сили-кагслях оставалась одинаковой. Этот факт может быть объяснен различным механизмом адсорбции данных примесей на силикагеле. При этом зависимость адсорбции триэтокеифос-фипа от количества гидроксилышх групп на поверхности еиликагеля свидетельствует об известной специфической адсорбции кислородсодержащих соединений на силикагелях. Независимость адсорбции FeCla от состояния поверхности может рассматриваться как один из признаков физической адсорбции. Обязательным условием для сравнения абсолютных значений емкостей является наличие высокочистых сорбентов и поверхностей. [16]
Первые же исследования в области адсорбции радиоактивных микропримесей установили многообразие ендов адсорбции для микроконцентрационных систем, особенно для ограниченно растворимых примесей. Было найдено, что примеси в разбавленных растворах могут находиться в различной физико-химической форме. Поэтому наряду с молекулярной адсорбцией в ряде неорганических систем имеют место ионообменный и хемосорбниошшй механизмы адсорбции. Стало очевидным, что границы области Генри для неорганических систем необычайно узки, п отличие от органических смесей, я взаимное влияние микро примесей проявляется уже на уровне 1 10 - 4 % и даже на уровне 1 10 - 10 % для систем электролитов. [17]
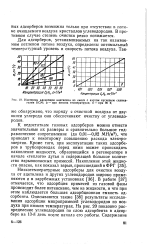 |
Изотермы адсороции ацетилена из смеси с азотом кусковым силика-гелем КСМ. а - при низких температурах. б - при 90 К. [18] |
В работе [37] отмечается, что адсорбция примесей из газовой фазы происходит более интенсивно, чем из жидкости, и что при этом наблюдается большая адсорбционная емкость адсорбента. Описываются также [38] результаты исследования адсорбции микропримесей углеводородов из воздуха при низких температурах. На рис. 20 показано распределение углеводородов по слою адсорбента в адсорбере на 13 - й день после начала его работы. [19]
Равновесие между различными формами примеси может легко сдвигаться при небольшом изменении концентрации раствора, а тем более при внесении хотя бы небольших количеств других веществ. Поскольку величина адсорбции является функцией физико-химического состояния вещества, адсорбция микропримеси может характеризоваться различными константами адсорбционного равновесия. Поэтому экспериментальные данные по адсорбции микропримесей, особенно труднорастворимых и легкогидролизуемых, в водных растворах изобилуют самыми разнообразными зависимостями, прежде всего от величины рН и свойств поверхности адсорбента. Поведение микропримесей в сорбциопных системах, как правило, аномально. [20]
Сорбция микропримеси фосфора ( в виде РС13) в трихлор-силапе неэффективна на силикягеле и более или менее эффективна на алюмогеле. Последнее обстоятельство зависит от соотношения двух факторов: кратности подавления адсорбции микропримеси РС13 в растворе SiHCl3 и от величины их относительной сорбции на алюмогеле. Опыт по сорбционной очистке SillCh от микропримеси Р полностью подтверждает высказанное предположение. [21]
Высокочистые растворы при хранении обычно изменяются. Эти изменения возникают в результате следующих трех процессов: 1) загрязнение материалом сосуда, в котором хранят раствор; 2) адсорбция микропримесей раствора на стенках сосуда и 3) загрязнение раствор а из-за десорбции ионов, ранее адсорбированных стенками сосуда. [22]
Высокочистые растворы при хранении обычно изменяются. Эти изменения возникают в результате следующих трех процессов: 1) загрязнение материалом сосуда, в котором хранят раствор; 2) адсорбция микропримесей раствора на стенках сосуда и 3) загрязнение раствора из-за десорбции ионов, ранее адсорбированных стенками сосуда. [23]
Динамика адсорбционного разделения бинарной смеси газов, обладающих соизмеримой сорбируемостью ( например, при адсорбционном разделении воздуха), существенно отличается от традиционной задачи динамики адсорбции микропримеси из малосорбирующего газа-носителя. Это отличие проявляется в возникновении переменной скорости потока газа вдоль зернистого слоя адсорбента. При вытеснении менее сорбируемого компонента более сорбируемым ( стадия адсорбции) скорость потока убывает по направлению движения разделяемого воздуха, что приводит к дополнительному сжатию адсорбционного фронта. При вытеснении более сорбируемого компонента менее сорбируемым [ процесс регенерации) скорость потока нарастает по длине слоя, что приводит к размытию фронта адсорбции. [24]
Равновесие между различными формами примеси может легко сдвигаться при небольшом изменении концентрации раствора, а тем более при внесении хотя бы небольших количеств других веществ. Поскольку величина адсорбции является функцией физико-химического состояния вещества, адсорбция микропримеси может характеризоваться различными константами адсорбционного равновесия. Поэтому экспериментальные данные по адсорбции микропримесей, особенно труднорастворимых и легкогидролизуемых, в водных растворах изобилуют самыми разнообразными зависимостями, прежде всего от величины рН и свойств поверхности адсорбента. Поведение микропримесей в сорбциопных системах, как правило, аномально. [25]
В качестве исследуемых объектов для проведения глубокой очистки были выбраны тетрахлорид кремния с примесью треххлористого железа и триэтоксисилан с примесью три-этилфосфита. Первый объект представляет собой систему неорганических веществ, второй - элементоорганическую. В последней работе было установлено, что максимальной емкостью по микропримесям обладает активная окись алюминия и силикагель АСМ. С этой целью была исследована адсорбция микропримеси Ре С1з из SiCU и примеси Р ( ОС2Н5) 3 из 5Ш ( ОС2Н5) з при температуре 20Э в интервале концентраций 1.10 - 4 - 1.10 - 6 вес. Последний образец был получен нами из особо чистого тетрахлорида кремния при проведении гидролиза в неблагоприятных условиях, в среде хлорида, а не в водной среде. Это было сделано в целях выяснения влияния условий проведения гидролиза тетрахлорида кремния на величину и свойства поверхности полученного силикагеля. [26]
Исследован процесс отмывки активированного угля БАУ от минеральных примесей, железа, алюминия, кальция, магния, марганца, титана, меди особо чистой соляной кислотой и водой при температурах 20, 50, 88 С, концентрациях кислоты 5, 20 и 36 % и скоростях потока 0.5, 1.2 и 3.4 л / мин. Установлено наличие экстремумов на выходных кривых вымывания, объясняемое авторами явлением возрастания концентраций примесей в растворе по мере продвижения раствора в глубь зерна. Установлена необратимость адсорбции хлоридов железа и меди на угле, объясняемая образованием соединений внедрения. Рекомендовано контролировать отмывку по анализу в элюате примесей, не образующих соединений внедрения. С применением метода радиоактивных индикаторов определена адсорбция микропримесей хлоридов железа, фосфора и мышьяка из хлоридов кремния и четы-реххлористого углерода на особо чистых силикагелях. Установлено совпадение абсолютных изотерм адсорбции на силикагелях разного происхождения. [27]
Страницы: 1 2