Адсорбция - бром
Cтраница 1
Адсорбция брома, как правило, сопровождается разрушением кристаллической решетки. При близкой химической структуре образование комплексов с бромом аморфными образцами полимера сопровождается значительно большим возрастанием проводимости, чем кристаллическими. [1]
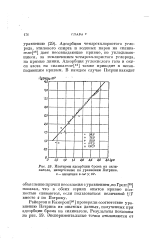 |
Изотермы адсорбции брома на силикагеле, начерченные по уравнению Пэтрика. - адсорбция в х 1 4. [2] |
Райерсон и Камерон [36 ] проверяли соответствие уравнению Пэтрика их опытных данных, полученных при адсорбции брома на силикагеле. [3]
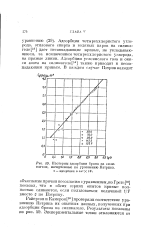 |
Изотермы адсорбции брома на оили-кагеле, начерченные по уравнению Патрика, в - адсорбция в см3 X Ю1. [4] |
Райерсон и Камерон [36] проверяли соответствие уравнению Патрика их опытных данных, полученных при адсорбции брома на силикагеле. [5]
Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на силика-геле. Брунауер и Эммет [7.] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить п-оо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. [6]
К рассмотренным здесь зависимостям можно было бы прибавить ряд других, в частности эмпирически установленную в [112] линейную зависимость между относительной адсорбцией брома ( и иода) в присутствии двух солей. [7]
Химической структурой и, в частности, наличием и размером боковых заместителей определяется и характер изменения полупроводниковых свойств полисопряженных систем при образовании комплексов с галоидами. Так, адсорбция брома сопровождается резким повышением проводимости ( 10 порядков. При переходе от полимера, полученного на основе глиоксаля, к полимерам, полученным на основе диацетила и особенно бензила, эффективность адсорбции ( в смысле увеличения проводимости) резко уменьшается. Мы объясняем это стерическими затруднениями для образования мостиков между участками сопряжения, создаваемыми объемистыми заместителями. [8]
Данные, приведенные в табл. 5.1, довольно хорошо согласуются с результатами, полученными другими методами. Стирнс и Джонсон 3 измеряли теплоты адсорбции брома на ряде саж. По полученным данным, соответствующим полному насыщению реакционноспо-собных участков, и по значениям удельной поверхности саж можно легко рассчлгать концентрацию активных ( по отношению к брому) участков на поверхности частиц сажи. Они также исследовали поведение тех же са ж в вулканизатах бутадиен-стирольного каучука при различных степенях наполнения; по деформационным свойствам и содержанию связанной серы в вулканизатах авторы рассчитали количество серы, химически связанной с поверхностью сажи. В табл. 5.2 приведено сравнение рассчитанных по их данным значений концентрации сцеплений с полученными ранее величинами. [9]
Затем в цилиндр с парами брома насыпают 10 г гранулированного активированного угля и энергично встряхивают цилиндр с содержимым. Бурая окраска паров брома исчезает в результате адсорбции брома активированным углем. [10]
При е 1, или Е, EL уравнения ( 38) и ( 41) описывают изотермы типа III. Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на еилика-геле. Брунауер и Эммет [7] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить поо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. Это значение представляет, однако, теплоту адсорбции при образовании лишь части мономолекулярного слоя, и величина Ег - средняя теплота адсорбции для всего первого слоя - может быть меньше этого значения. Если это верно, то из уравнения ( 38) следует, что v - vm при р0 5р0, и следовательно, константа vm может быть найдена из любой изотермы. Если вычислять величину поверхности, покрытой молекулами брома, исходя из плотности жидкого брома, то для удельной поверхности силикагеля получается значение 470 л 2 / г, что находится в превосходном согласии с величиной 500 л 2 / г, найденной из изотерм типа / / для азота, аргона, кислорода, окиси углерода и сернистого га. [11]
Следует ожидать, что возможность образования при адсорбции проводящих мостиков и их эффективность в значительной степени будут определяться как химическим строением макромолекул полимера, так и его надмолекулярной структурой. Действительно, на примере полишиффовых оснований мы показали [54], что в наибольшей степени повышение проводимости имеет место при адсорбции брома полимерами, у которых в цепи полисопряжения нет больших заместителей. Наличие СН3 - групп уменьшает эффективность адсорбции брома, в случае же, когда атомы водорода замещены фенильны-ми радикалами, эффект адсорбции галоида проявляется еще слабее. [12]
Заметим, что в случае экспозиции кристаллов AgCl и AgBr в парах галогенов электропроводность кристаллов возрастает пропорционально корню квадратному из давления пара. Эффекты, наблюдаемые в нестехиометрических кристаллах AgBr, содержащих избыток брома, - возникновение дырочной проводимости и поляризационные явления аналогичной природы - указывают на образование и миграцию положительных электронных вакансий - дырок. Ясно, что адсорбция брома на внешней или внутренней поверхности как-то интерферирует с миграцией подвижных ионов серебра, тормозя последнюю. [13]
Следует ожидать, что возможность образования при адсорбции проводящих мостиков и их эффективность в значительной степени будут определяться как химическим строением макромолекул полимера, так и его надмолекулярной структурой. Действительно, на примере полишиффовых оснований мы показали [54], что в наибольшей степени повышение проводимости имеет место при адсорбции брома полимерами, у которых в цепи полисопряжения нет больших заместителей. Наличие СН3 - групп уменьшает эффективность адсорбции брома, в случае же, когда атомы водорода замещены фенильны-ми радикалами, эффект адсорбции галоида проявляется еще слабее. [14]
Райерсон и Камерон измерили также адсорбцию иода на силикагеле. Эти результаты удивительны, так как были получены очень малые значения адсорбции. Пользуясь значением поверхности, полученным из изотерм адсорбции брома, и предполагая, что упаковка молекул иода на поверхности та же, что и в жидком состоянии, находим vm равным 2 93 миллимоля иода на грамм силикагеля. Это указывает на то, что силы адсорбции значительно слабее, чем силы, действующие между молекулами иода в жидком состоянии. [15]
Страницы: 1 2