Адсорбция - смесь
Cтраница 4
СО и при адсорбции смеси 2СО: 102 на окисленной поверхности, вероятно, достигается одно и то же адсорбированное состояние кислорода. Отмечая, что теплота адсорбции С02 на Мп2О3 очень хорошо соответствует теплоте диссоциации карбоната марганца, исследователи пришли к выводу, что адсорбированным состоянием, свойственным для таких процессов, является поверхностный карбонат-ион. Было высказано предположение, что окись углерода взаимодействует с кислородом кристаллической решетки окисла металла, образуя при этом поверхностный карбонат-ион, а также, что ненасыщенность в отношении кислорода после адсорбции СО следует считать результатом появления анионной вакансии при адсорбции СО. [46]
Первые сообщения по адсорбции смесей были сделаны в работе Фрейндлиха и Мазиуса [262], в которой были сформулированы правила вытеснения и было показано, что оба компонента в смеси адсорбируются меньше, чем каждый компонент в отдельности, причем из смеси преимущественно адсорбируется тот компонент, который сильнее адсорбируется из своего индивидуального раствора. При очень большой разнице в поглощении двух компонентов смеси может наступить полное отравление адсорбента по отношению к слабо адсорбирующемуся компоненту. [47]
Стройной теории по адсорбции смеси газов до сих пор не создано. Однако авторы сами отмечают, что рассмотренная приближенная статистическая теория адсорбции бинарных смесей находится в полуколичественном согласии с результатами опытов. Сложность учета взаимного влияния адсорбированных молекул и селективности поверхности заставляет до настоящего времени признать опыт единственно надежным средством для расчета адсорбции многокомпонентных смесей. [48]
Экспериментальные данные по адсорбции смесей паров на микропористых адсорбентах, полученные Б. П. Берингом, В. В. Серпин-ским и С. И. Суриковой, послужили веским дополнительным аргументом для утверждения теории объемного заполнения. [49]
В практических условиях адсорбция смесей паров органических растворителей с целью их рекуперации производится до момента проскока за слой паров менее сорбируемого вещества. [50]
Поскольку в случае адсорбции смесей изотерма Ленгмюра связывает поверхностные концентрации с концентрациями в газовой или жидкой фазе, мы имеем все данные для теоретического расчета скоростей. [51]
Импульсно-динамический метод изучения адсорбции смесей из потока основан на сочетании проявительной и вакантной хроматографии. Сущность его заключается в следующем. Газ-носитель, насыщенный парами веществ, адсорбция которых изучается, пропускают через микрореактор, хроматогра-фическую колонку и детектор. После установления равновесия через дозатор на адсорбент вводится некоторое количество вытеснителя. Десорбирующиеся при этом вещества уносятся потоком газа-носителя в хроматографическую колонку, а затем в детектор, где разделяются и детектируются. Одновременно с процессом вытеснения начинается элюирование вытеснителя с адсорбента, причем на освобождающихся центрах адсорбируются пары веществ, находящихся в потоке. Если в газовой фазе присутствуют пары одного вещества и адсорбция осуществляется с достаточно большой скоростью, вакантная кривая характеризует десорбцию вытеснителя со всей поверхности адсорбента. Если же газ-носитель насыщен парами смеси веществ, то вакантные кривые характеризуют десорбцию вытеснителя с центров, на которых адсорбируются компоненты смеси. Схема установки для изучения адсорбции импульсно-динамическим методом ( рис. 1) представляет схему обычного газового хроматографа с двумя параллельными потоками, в один из которых подключается микрореактор с адсорбентом. Часть газа-носителя пускается при помощи байпасного вентиля 4 через термостатируемый сатуратор 2, в котором он насыщается парами веществ, адсорбция которых изучается. Микрореактор 9 представляет трубку из нержавеющей стали длиной 10 мм и внутренним диаметром 3 мм. Он помещен в воздушный термостат А с терморегулированием от 50 до 350 и максимальной скоростью нагрева 20 в минуту. [52]
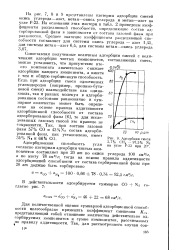 |
Адсорбция смеси 2 7 % СН4 - 97 3 % N2 на угле F-23 при 20. [53] |
Сопоставляя полученные величины адсорбции смесей с величинами адсорбции чистых компонентов, составляющих смесь, можно установить, что присутствие вто-ого компонента значительно снижает адсорбцию каждого компонента, а вместе с тем и общую сорбционную способность. Если при адсорбции смеси однотипных углеводородов ( например, пропано-бута-новой смеси) взаимодействие как одинаковых, так и разных молекул в адсорбированном состоянии равнозначно и суммарное количество может быть определено на основе правила аддитивности адсорбционной способности от состава адсорбированной фазы [6], то для исследованных газовых смесей это правило не сохраняется. Так, при составе газовой фазы 57 % СО и 43 % N состав адсорбированной фазы, как установлено, имеет 34 % N2 и 66 % СО. [54]
Для описания динамики адсорбции смесей в движущемся слое использованы математические модели, аналогичные моделям одного компонента. При составлении этих моделей принимается, что с верха адсорбционной колонны определенной высоты подается чистый или частично заполненный сорбируемым веществом адсорбент. [55]
Расчетную суммарную величину адсорбции смесей ( о а, а2) определяли по уравнениям Марк-гема - Бентона: расч. [56]
Страницы: 1 2 3 4