Адсорбция - алифатический спирт
Cтраница 1
Адсорбция алифатических спиртов на границе ртуть - раствор впервые была изучена А. Н. Фрумкиным [457]; впоследствии были проведены измерения емкости двойного слоя на твердых электродах - свинце и платине [458-459], доказавшие адсорбцию молекул спирта ( изучался амиловый спирт) на электроде вблизи потенциала нулевого заряда. [1]
При изучении адсорбции алифатических спиртов на поверхности цинка электрохимическим методом [28] было обнаружено, что влияние спиртов резко меняется в зависимости от концентрации сернокислого цинка, причем влияние концентрации электролита проявляется двояким образом. С одной стороны, при увеличении концентрации электролита происходит усиление адсорбции органического вещества на поверхности металла, вследствие чего в концентрированных растворах оказывают влияние столь малые концентрации добавок, которые в разбавленных растворах почти совершенно не действуют. С другой стороны, увеличение концентрации соли в растворе сильно уменьшает скорость адсорбции поверхностно-активного вещества. [2]
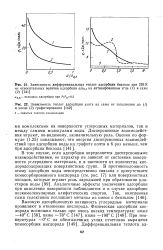
Можно ожидать, что форма изотермы адсорбции алифатических спиртов с короткой цепью будет заметно зависеть от природы поверхности твердого тела. Это подтверждается результатами исследования [70] адсорбции н-пропилового спирта на восстановленном и окисленном железе и на окисях железа. Присутствие окисей ( рис. 46) приводит к резкому изгибу изотермы. Даже на дегидратированном кремнеземе [72] взаимодействие ( через водородную связь) достаточно сильно, чтобы вызвать локализацию адсорбированных молекул на поверхности. [3]
Поскольку в последнее время получены данные по влиянию температуры на адсорбцию алифатических спиртов [3] и жирных кислот [7], представляет интерес продолжение этих исследований для органических веществе другими функциональными группами; в настоящем сообщении рассматривается температурная зависимость адсорбции метилэтил - и диэтилкетонов на ртути. Сведения об адсорбционном поведении кетонов на ртутном электроде изложены в [8-11], однако из-за различия методов изучения и состава электролита сопоставление их затруднительно. [4]
В этих работах было установлено, что для таких металлов, как свинец, таллий, кадмий, серебро, галлий, наблюдается явно выраженная зависимость адсорбции алифатических спиртов от заряда поверхности. Для всех исследованных металлов на кривых зависимости дифференциальной емкости от потенциала в присутствии поверхностно-активного органического вещества наблюдается область низких значений емкости и пики адсорбции - десорбции. [5]
 |
Кривые емкости. [6] |
Значительная часть перечисленных работ по адсорбции органических веществ на твердых металлах носила качественный характер, и на основе данных этих работ была невозможна количественная проверка применимости теории Фрумкина - Дамаскина [55, 56] к описанию адсорбционных явлений на твердых металлах. Лишь в последние годы проведено систематическое исследование адсорбции алифатических спиртов на свинцовом [63, 64] и висмутовом [41, 65-67] электродах. В указанных работах на свинце и висмуте показано хорошее соответствие между рассчитанными из теории Фрумкина - Дамаскина и из экспериментальных данных изотерм адсорбции, С - ф-кривых и зависимостей заполнения поверхности от потенциала. [7]
Изучение условий, изменяющих скорость адсорбции поверхностно-активных веществ, имеет большое значение для процесса электроосаждения металла, поскольку скоростью адсорбции определяется самоприспосабливающаяся скорость осаждения и, следовательно, характер электролитического осадка металла на катоде. Поэтому экспериментальные результаты изучения влияния концентрации электролита на скорость адсорбции алифатических спиртов при злектроосаж-дении цинка будут рассмотрены подробно. [8]
В том случае, если адсорбция определяется дисперсионными взаимодействиями, ее характер не зависит от состояния поверхности углеродного материала, и в частности от количества кислородсодержащих поверхностных групп. Аналогичные эффекты увеличения адсорбции при окислении поверхности наблюдаются и в случае адсорбции низкомолекулярных алифатических спиртов. [10]
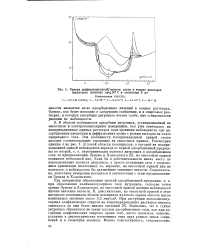 |
Кривые диффйренциальной емкости ртути в водных растворах перхлората тропилия при 200 С и амплитуде 8 мв. [11] |
Зумана и Ходковского, на емкостной кривой должны наблюдаться низкие значения емкости. Возможно, что в случае дитропила образуются не такие толстые адсорбционные слои, как при адсорбции алифатических спиртов; кроме того, могло сказаться, конечно, различие в диэлектрических постоянных этих двух разных типов соединений и в геометрии молекул. [12]
В случае добавления тиомочевины скорость адсорбции получается меньшей, хотя она значительно выше, чем при адсорбции алифатических спиртов на цинке. [13]
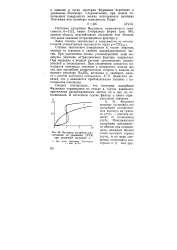 |
Изотермы адсорбции, рас - точки нулевого заряда считанные по уравнению у. [14] |
Степень заполнения поверхности 0, таким образом, зависит от строения и свойств адсорбирующихся частиц. При увеличении длины углеводородной цепи молекулы значение аттракционного фактора возрастает. При введении в водный раствор органических растворителей Y уменьшается. При увеличении катодного потенциала электрода значение Y возрастает, иногда же, как при адсорбции алифатических спиртов и аминов из водного раствора N32864, величина - у. Y изменяется приблизительно линейно с потенциалом электрода. [15]
Страницы: 1