Адсорбция - этанол
Cтраница 2
Определены изотермы адсорбции этанола на активированном угле и силикагеле. [16]
На расположение и форму всей электрокапиллярной кривой сильное влияние оказывает изменение природы раствора. Рассчитанная по уравнению ( IV-71) адсорбция этанола на поверхности ртути всегда положительна, и ее зависимость от состава раствора напоминает аналогичную зависимость для поверхности раздела раствор - воздух. [17]
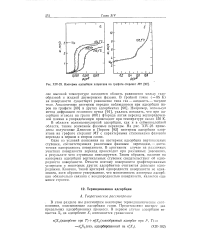
Из-за разного влияния потенциала электрода на различные стадии превращения исходных органических молекул и продуктов хемосорбции с изменением потенциала меняется как общее количество хемосорбированного вещества, так и соотношение различных частиц на поверхности. Это демонстрирует рис. 3.11, где приведены результаты исследования адсорбции этанола на Pt-электроде в сернокислом растворе импульсными методами ( А. [18]
 |
Изотермы адсорбции хлорэтана на графите стерлинг МТ. [19] |
В тройной точке ( - 85 К) на поверхности существует равновесие типа газ - жидкость - твердое тело. Например, используя метод дифракции гелиевого пучка [91], удалось показать, что при адсорбции этанола на грани ( 001) фторида лития переход неупорядоченной пленки в упорядоченную происходит при температуре около 150 К. [20]
 |
Кривые зависимости заряда поверхности ртути в насыщенных при 30 С водно-этаноловых растворах хлористого аммония от потенциала относительно хлорсеребряного электрода в том же растворе. [21] |
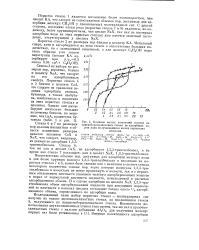
Истинные изотермы адсорбции этанола из электрокапиллярных измерений рассчитать невозможно, поскольку распределение этанола в адсорбционном слое неизвестно. Вследствие этого интерес представляет сопоставление изотерм адсорбции, вычисленных из электрокапиллярных кривых, с изотермами адсорбции этанола по измерениям дифференциальной емкости ртути в контакте с водно-этаноловыми растворами хлористого аммония. [22]
 |
Влияние малых изменений состава на-триевоборосшшкатных стекол на адсорбцию паров воды получающимися из них пористыми стеклами. [23] |
Стекло 3 из набора по размерам пор, вероятно, близко к цеолиту NaA, что следует из его адсорбционных свойств. Пористые стекла 4 и 5 близки к цеолиту СаА, что следует из сравнения величин адсорбции этанола, бутанола, а также изобута-на, изобутанола и изооктана на этих пористых стеклах и цеолитах. [24]
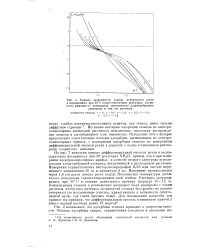
На рис. 1 показана серия полученных таким образом изотерм адсорбции этанола на ртути из насыщенных при 30 водно-этаноловых растворов хлористого аммония. В согласии с наблюдениями над множеством других органических соединений, потенциал ртути очень сильно влияет на адсорбцию этанола на ртути. [25]
Сорбция метилового спирта на нем почти вдвое меньше сорбции воды. Функция распределения объема пор по радиусу у этого образца шире, чем у 30 / 2: адсорбция этанола составляет 15 - 20 % от адсорбции метанола. [26]
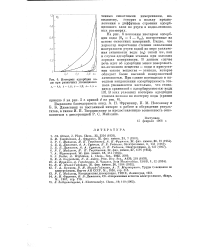 |
Изотермы адсорбции воды при различных [ потенциалах. [27] |
На рис. 6 показаны изотермы адсорбции воды ( 9В 1 - 6СП), построенные на основе емкостных измерений. Видно, что характер нарастания степени заполнения поверхности ртути водой по мере увеличения активности воды ( яв) такой же, как в случае адсорбции этанола при высоких зарядах поверхности. В данном случае речь идет об адсорбции менее поверхностно-активного вещества - воды в присутствии такого вев ] ества - этанола, которое обладает более высокой поверхностной активностью. [28]
Размытие хвоста пика обычно вызывается адсорбцией растворенного вещества твердым носителем, на который нанесена неподвижная фаза. Таким образом, при хроматографическом анализе этанола на набивке, состоящей из целита и силикона, асимметрия пика должна вызываться не взаимодействием между этанолом и силиконом, а адсорбцией этанола на целите. Основная масса растворенного вещества непрочно связывается с распределяющей жидкостью, но небольшие количества его крепко удерживаются целитом и элюируются медленно. Из-за этого и происходит размытие хвоста пика. Найт [68] обнаружил, что размытие хвоста пика можно уменьшить, избегая тех концентраций, при которых адсорбционная изотерма сильно искривляется. Практически этого легче всего достигнуть, поддерживая все время низкую концентрацию вещества на колонке. [29]
Гринлер установил, что молекулярно адсорбированный спирт удаляется при откачке образца до 35 С. После удаления слабо связанных с поверхностью молекул спирта в спектре оставались полосы поглощения метоксильных групп 1190, 1100 и 1030 см-1 в случае адсорбции метанола и полосы поглощения этоксильных групп 1080, ИЗО и 1170 см-1 в случае адсорбции этанола. [30]
Страницы: 1 2 3