Адсорбция - благородный газ
Cтраница 2
Эти кривые лежат заметно выше соответствующих экспериментальных значений. Таким образом, термодинамические характеристики адсорбции благородных газов на базисной грани графита, оцененные указанным выше путем на основании свойств адсорбата и адсорбента, взятых в отдельности, заметно отличаются от соответствующих экспериментальных значений. Рассмотрим возможные причины этого расхождения. [16]
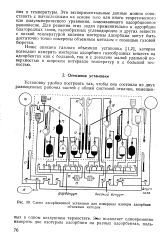 |
Схема адсорбционной установки для измерения изотерм адсорбции. [17] |
Для решения этих задач применительно к адсорбции благородных газов, газообразных углеводородов и других веществ с низкой температурой кипения изотермы адсорбции могут быть достаточно точно измерены объемным методом с помощью газовой бюретки. [18]
 |
Рассчитанные ( линии и экспериментальные ( точки значения константы Генри Kns, с, i ( см3 / г при разных температурах для адсорбции благородных газов цеолитом NaX. [19] |
Расчет Кns c tc использованием найденных так параметров атом-ионного ( катионного) потенциала дает близкие к имеющимся экспериментальным значениям результаты для цеолита КХ с тем же отношением Si / Al. При изменении этого отношения, например при переходе от адсорбции благородных газов цеолитом NaX к адсорбции цеолитом NaY, коэффициент 3 изменяется. [20]
По третьему методу [ см. реакцию (4.25) ] полное разложение происходит за 7 сек в инконелевой трубке при 1000 С. Возможно образование некоторого количества NO2, которая может быть удалена перед адсорбцией благородных газов. [21]
Необходимое для эмиссии поле может сильно повлиять на поверхностное распределение слабо адсорбированного газа. Роль такого рода эффектов поля можно оценить только экспериментально. Влияние адсорбции благородного газа на электронную эмиссию может оказаться недостаточным для четких наблюдений. Предшествующее исследование Миньоле [54] с напыленными пленками, в котором были установлены значительные изменения работы выхода при физической адсорбции, свидетельствует, что никакие препятствия, обусловленные недостатком чувствительности, не возникают. [22]
В любом процессе адсорбции обязательно участвуют неполярные силы Ван-дер - Ваальса и силы отталкивания. Однако случаи, когда действуют только эти две силы, являются весьма немногочисленными. Примером их служит адсорбция благородных газов на неполярных диэлектрических поверхностях. [23]
Этим сферам была приписана повышенная поляризуемость за счет связи с четвертичным атомом углерода, который как таковой в расчете не учитывался. Однако в дальнейшем необходимо использовать более точную модель цеолита, разработанную в описанном выше расчете для адсорбции благородных газов [180], и разработать более точную модель для сложных молекул углеводородов. Поэтому в следующей работе этой серии [183] для вычисления термодинамических характеристик удерживания углеводорода цеолитами было применено описанное выше для удерживания на ГТС атом-атомное ( атом-ионное) приближение. [24]
Следует заметить, что это различие далеко не всегда может быть четко проведено. В крайних случаях физическая адсорбция, определяемая лишь вандерваальсовыми силами, характеризуется: 1) хорошей обратимостью; 2) отсутствием стехиометрических соотношений; 3) уменьшением адсорбции при повышении температуры; 4) близостью тепловых эффектов адсорбции к теплотам сжижения или испарения; такова адсорбция благородных газов или гексана на угле. В других крайних случаях химическая адсорбция осуществляется только путем химического взаимодействия, например, между кислородом и вольфрамом или кислородом и серебром при повышенных температурах; в этом случае: 1) адсорбция почти необратима; 2) тепловой эффект близок к энергии образования химических соединений ( около 100 ккал / моль и выше); 3) величина адсорбции увеличивается с температурой и др. Обычно осуществляются промежуточные случаи, когда основная масса адсорбированного вещества связывается сравнительно слабо, а последние следы связаны прочно и могут быть удалены лишь путем длительного прогревания и откачивания. Кислород на металлах или водород на никеле адсорбируется при низких температурах физически ввиду малой скорости химической реакции при этих температурах. Однако при повышении температуры начинает протекать адсорбция с заметной энергией активации ( активированная адсорбция) по типу химических реакций. В определенном интервале повышения температур прирост химической адсорбции ( или хемосорбции) перекрывает падение физической адсорбции и на кривой температурной зависимости адсорбции возникает промежуточный максимум, характерный для наличия активированной адсорбции. [25]
 |
Установка для удерживания радиоактивных благородных газов ( фотография Lurgi. [26] |
Длительное удерживание этих благородных газов на адсорбентах в больших концентрациях не представляется возможным. Однако, если время удерживания в одном адсорбере, снаряженном активным углем, достаточно велико по сравнению с периодом полураспада изотопа, то на угле накапливаются твердые продукты, образованные из этих короткоживущих изотопов благородных газов. Отходящий воздух следует дополнительно тщательно осушать с помощью осушителей или конденсацией, чтобы исключить отрицательное влияние влаги на адсорбцию благородных газов, обладающих плохой адсорбируемостью. [27]
Известны многочисленные экспериментальные данные, указывающие на многоступенчатый характер изотерм адсорбции. В работах де - Бура было показано, что ступени на изотермах адсорбции возникают в результате двумерной конденсации на неоднородной поверхности адсорбента. Однако существует ряд данных, которые не могут быть объяснены двумерной конденсацией. В нашей лаборатории проводится исследование адсорбции благородных газов на поверхности свежего скола кристаллов исландского шпата. Изотермы адсорбции Аг, Хе, Не и N2 в интервале давлений 1 10 - 3 - 40 мм рт. ст. при комнатной температуре имеют ясно выраженный ступенчатый характер. Изменение величины адсорбции в 2 - 3 раза происходит при изменении давления на - 0 2 мм рт. ст. При исследуемых давлениях температура опыта была значительно выше критической, и поэтому ступенчатый характер изотерм не может быть объяснен двумерной конденсацией на поверхности кристаллов. [28]
Поверхностный потенциал, наблюдаемый при адсорбции СО на пленках меди, серебра и золота, оказывается положительным [18] в отличие от ПП на пленках переходных металлов. Теплоты адсорбции в таких системах неизменно малы, и обычно предполагается, что здесь имеет место физическая адсорбция. В самом деле, положительные значения 1111 на металлах характерны для физической адсорбции, а взаимодействие ксенон - металл сопровождается довольно большими изменениями характеристик. В абсолютно всех изученных случаях не вызывающей сомнений физической адсорбции поверхностный потенциал имел положительное значение. Однако расчет [19] говорит о том, что положительные значения ПП ( по крайней мере, при адсорбции благородных газов) могут равным образом быть результатом поляризации. [29]
Мы видим, что захвата радона не происходит только в случае аммиака. Как НС1, так и НВг и H2S захватывают при перекристаллизации заметные количества радона. Скорость перекристаллизации незначительна: за 2 часа успевает перекристаллизоваться лишь небольшая часть кристаллов; при более длительной перекристаллизации захват радона был бы количественным. Следовательно, количество перешедшего в кристаллы радона сильно зависит от времени. Это доказывает, что радон захватывается именно при перекристаллизации, так как адсорбция протекает очень быстро. Кроме того, адсорбция благородных газов всегда является обратимой. [30]
Страницы: 1 2 3