Изучение - комплексообразование
Cтраница 1
Изучение комплексообразования в системах на основе тригало-генидов элементов Ш и Ч групп представляет большой интерес, так как в них должна сильно сказываться конкуренция в процессах образования соединений ионного и донорно-акцепторного типа. [1]
Изучение комплексообразования Со ( II) осложняется переходом Со ( П) - - Со ( III), быстро протекающим в присутствии окислителя и лигандов. Смещение равновесия комплексообразования в сторону образования комплексов Со ( III) связано с большей термодинамической устойчивостью комплексов Со ( III) по сравнению с комплексами Со ( II) ( в соответствии с уравнением Нернста [ 3, с. Такое соотношение в устойчивости объясняется не только большим вкладом ( при прочих равных условиях) электростатической составляющей в химическую связь в случае комплексов трехзарядного Со3, но и - электронной конфигурацией Со3, в большей мере обеспечивающей ковалент-ную стабильность комплекса, чем ион Со2 с сР - электронной конфигурацией. [2]
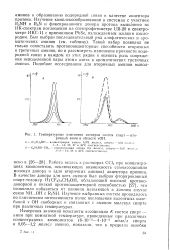 |
Температурные изменения спектров систем спирт - вторичный амин в области vOH. [3] |
Изучение комплексообразования в системах с участием R2NH и R3N и фиксированного донора протона выполнено по ИК-спектрам поглощения на спектрофотометре UR-20 и спектрометре ИКС-11 с приемником PbSe, охлаждаемым жидким кислородом. Такой набор позволил не только сопоставить протоноакцепторные способности вторичных и третичных аминов, но и рассмотреть изменение прочности водородной связи в каждом из этих рядов и оценить роль сопряжения неподеленной пары атома азота в ароматических третичных аминах. [4]
Изучение комплексообразования в системах вольфрам - пирокатехиновый фиолетовый, ниобий - пирокатехиновый фиолетовый. [5]
Изучение комплексообразования в растворах прежде всего начинается с выяснения количества и типа образующихся комплексов и определения их констант устойчивости. Количественному изучению системы, в которой происходит образование комплексных соединений, как правило, предшествует качественное. На этой стадии исследования выясняются вопросы - имеет ли место процесс комплексообразования, и если имеет, то какие компоненты системы принимают в них участие. Растворитель практически всегда участвует в процессах комплексообразования и поэтому такой вопрос не ставится. Например, при добавлении к водному раствору медного купороса раствора аммиака окраска изменяется от голубой до глубокой синей, а при добавлении к раствору РеС13 ионов SCN - появляется кроваво-красная окраска. В других случаях для суждения об участии в комплексо-образовании используют аналитические реакций на тот или иной ион или молекулу. Если ионы или молекулы принимают участие в образовании прочного комплексного соединения, то их не удается обнаружить при помощи качественных аналитических реакций. Характерные реакции на ион Fe3 со щелочью или с роданидом калия будут отрицательными. [6]
Изучение комплексообразования в сложном растворителе вода - монохлоруксусная кислота представляет интерес, потому что позволяет показать, как находят состав и определяют константы устойчивости комплексов в условиях, когда активность ионов водорода становится соизмеримой с величиной кажущейся константы диссоциации кислоты. [7]
Изучение комплексообразования осмия в сульфитсодержащих системах представляет интерес для координационной химии ввиду ограниченности сведений по сульфитокомплексам этого металла, а также для решения задач по извлечению осмия в технологической и в аналитической практике. [8]
Изучение комплексообразования ПЭ началось давно, и это наложило свой отпечаток на состояние и пути развития химии комплексов платиновых элементов. [9]
Для изучения комплексообразования исследования рекомендуют проводить несколькими методами. Надежными считаются константы, полученные различными методами и совпадающие по значению в пределах ошибки опыта. Силлен предложил делить методы исследования комплексообразования в растворах на три группы. [10]
Методически изучение комплексообразования ванадия ( III) и ванадия ( IV) проводили следующим образом: в растворы с различным соотношением винной кислоты и сернокислых солей ванадия вводили различные количества 0 1 М раствора едкого калия. [11]
При изучении комплексообразования в водных растворах широкое применение получил метод постоянной ионной силы, величина которой может быть различной ( от 0 1 до 4 м в зависимости от устойчивости образующихся в растворе комплексов. Для создания ионной среды обычно используется cwiblNJaClO, так как перхлорат - ион не образует комплексных соединений с большинством ионов металлов. [12]
При изучении комплексообразования и равновесий молекулярных форм в качестве Кс может использоваться изобестиче-ская точка. [13]
При изучении комплексообразования Ti4 с о-полифено-лами в различных органических растворителях было показано [229], что прочность комплексов возрастает в ряду вода ди. [14]
При изучении комплексообразования циркония-95 [104] с азотной кислотой ( при постоянной суммарной концентрации HN03 и НСЮ4, равной 2) удалось установить, что анионное поглощение начинается при ( 7нмо3 1 м - и не достигает своего предела в выбранных условиях. [15]
Страницы: 1 2 3 4