Возможность - сольватация
Cтраница 1
Возможность сольватации экстрагирующих комплексных кислот молекулами органического растворителя практически никогда не вызывала сомнений, а в настоящее время сольватация четко доказана. Этого нельзя сказать о гидратации комплексов, поскольку в ряде ранних работ ее ставили под сомнение ( см. Введение); ныне, однако, хорошо установлено, что в большинстве случаев извлекающиеся кислоты содержат в своем составе молекулы воды. [1]
Влияние второй и третьей оксигрупп объясняется усилением связи молекулы с водой и уменьшением возможности сольватации органическими растворителями. [2]
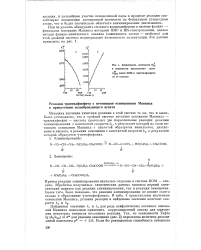 |
Зависимость плотности ( Л и показателя преломления света. [3] |
Нам не удалось обнаружить сильного взаимодействия в системе фосфит - фенольное основание Манниха методами ПМР и ИК-спектроскопии, однако методы физико-химического анализа ( зависимость состав - свойство) для этой двойной системы подтверждают возможность сольватации. [4]
Имеются данные о незначительном влиянии природы растворителя па скорость радикальных реакций. При этом обсуждается возможность сольватации свободных радикалов. В целом влияние природы растворителя на гемолитические реакции значительно ниже, чем на гетеролитические. [5]
По теории абсолютных скоростей реакций следует учитывать сольватацию исходных реагентов и переходного комплекса. IV) является возможность неравновесной сольватации переходного комплекса, которую обычно не принимают во внимание при трактовке экспериментальных закономерностей, хотя последние могут зависеть от нее. [6]
В заключение необходимо отметить, что при несомненной пользе рассмотрения проблемы сольватации переходного комплекса с чисто электростатических позиций оно безусловно не является единственно правильным. Следует, в частности, иметь в виду возможность сольватации переходного комплекса за счет образования водородных связей и донорно-акцепторных комплексов с молекулами растворителя. Уже тот факт, что значения дипольных моментов цхф при сольволизе трет - dHgCl в апротонных и гидроксил-содержащих растворителях различны, хотя для обоих случаев электростатическая теория оказывается справедливой, указывает на необходимость учитывать при обсуждении вопроса о сольватации переходного состояния и возможность образования водородных связей с растворителем. К сожалению, современное состояние теории таково, что рассмотрение эффектов сольватации переходного комплекса с учетом всех составляющих сейчас практически неосуществимо. [7]
Некоторые исследователи [56] считают возможным, что при перегруппировке Фаворского и некоторых конкурирующих с ней реакциях образуется не простая циклопропановая система ( см. выше), а промежуточный продукт, в котором сильно делокализо-ваны либо заряд [ 56а, б, в ], либо связи [ 56г ], либо, как в планар-ном резонансном гибриде XX, и то и другое одновременно. Поскольку такой промежуточный продукт обладает плоскостью симметрии, то ( если не рассматривать возможность асимметричной сольватации) он не способен к стереоспецифическим превращениям. Резонансные формы Г, Д и Е подразумевают, что С - О или Са - Са1 - связи имеют скорее я -, нежели о-характер. [8]
По механизму AAcl осуществляется также гидролиз и сольво-лиз галогенангидридов кислот в кислой среде. Реакция идет тем легче, чем выше кислотность среды и, следовательно, чем больше возможность сольватации отщепляющегося галогенид-иона Так как значение специфической сольватации возрастает по мере уменьшения объема сольватируемого аниона, реакции AAcl особенно характерны для фторангидридов. Повышение реакционной способности нуклеофильного реагента может привести к смене механизма, и реакция идет как нуклеофильное присоединение по карбонильной группе. [9]
Высоковакуумная техника всегда привлекала пристальное внимание электрохимиков, так как наиболее интересные электрохимические системы всегда обладают повышенной чувствительностью к присутствию даже следовых количеств воды. Такая чувствительность может быть обусловлена как реакциями воды с одним или несколькими видами исследуемых ионов, так и с возможностью интенсивной сольватации. Этим обстоятельством можно объяснить немыслимое разнообразие конлуктометричсских ячеек, разработанных специально для измерений в вакуумных системах. Кроме того, поскольку в большинстве электрохимических экспериментов электрическая проводимость определяется в виде функции от концентрации одной или нескольких компонентов, исследователи вложили много труда и изобретательности в разработку разнообразных устройств для разбавления, концентрирования и титрования растворов под вакуумом. [10]
Методом инфракрасной спектроскопии была исследована сольватация и гидратация экстрагирующихся соединений железа. Было показано, прежде всего, что молекулы органического растворителя и воды входят в состав этих соединений. Исследование возможности сольватации аниона FeQ4 - показало, что этот анион в экстрактах координацией о не сольватирован. [11]
Методом инфракрасной спектроскопии была исследована сольватация и гидратация экстрагирующихся соединений железа. Было показано, прежде всего, что молекулы органического растворителя и воды входят в состав этих соединений. Исследование возможности сольватации аниона РеС14 показало, что этот анион в экстрактах координационно не сольватирован. [12]
 |
Константы распределения бензидина. [13] |
Две легко гидратируемые группы ОН снижают сольватацию находящихся между ними СН2 - групп. Поэтому и для ряда гликолей гомологическая разность констант распределения довольно мала. С увеличением числа атомов углерода в молекуле гликоля расстояние, между группами ОН возрастает и при этом возможность сольватации увеличивается, это приводит к возрастанию гомологической разницы. [14]
При образовании водородных связей этот растворитель выступает как сильнейший акцептор. Сильное взаимодействие такого же типа, вероятно, происходит и в смесях диметилсульфоксида с метанолом, что уменьшает возможность сольватации метилат-ионов метанолом. [15]
Страницы: 1 2