Изучение - электрохимическое поведение
Cтраница 1
Изучение электрохимического поведения ( скорости коррозии, поляризационных характеристик) различных граней монокристалла затруднено несколькими обстоятельствами. Во-первых, нет уверенности в том, что исследуется совершенная грань, лишенная микрорельефа. Во-вторых, необходимо учитывать влияние природы раствора, взаимодействующего с поверхностью металла, пока теоретически не осмысленное. По этому поводу можно только заметить, что переход ионов металла в раствор сопровождается адсорбцией компонентов среды ( ионов, молекул растворителя), влияющей на скорость электродного процесса ( гл. В-третьих, при текущем процессе взаимодействия со средой исходная, даже совершенная, грань кристалла должна испортиться - на ней должен появиться рельеф, хотя бы отвечающий положению у полукристалла, которое определяет растворение металла посредством повторяющегося шага. Последнее обстоятельство имеет весьма большое значение. [1]
Изучение электрохимического поведения никеля, кобальта и железа показало, что в определенной для каждого металла области температур ( выше 100 С) система металл-раствор становится обратимой. Использованный в работе метод позволяет непосредственно измерять равновесные потенциалы металлов группы железа и на основании полученных данных определить значения равновесных потенциалов этих металлов для различных температур. Приведенные экспериментальные результаты показывают неправильность существующего до сих пор мнения о невозможности определения равновесных потенциалов переходных металлов прямым электрохимическим методом. [2]
Изучение электрохимического поведения радиоактивных изотопов очень важно как с практической, так и с теоретической точки зрения. Электрохимическими методами пользуются при выделении радиоактивных изотопов в состоянии большой химической и радиохимической чистоты, при приготовлении источников радиоактивных излучений путем нанесения на поверхность электрода любой величины тонкого и равномерного слоя радиоактивного изотопа. Электрохимические методы исследования используются при изучении химических и физико-химических свойств радиоактивных изотопов, находящихся в состоянии сильного разбавления. [3]
При изучении электрохимического поведения связи углерод-галоид на примере цис - и транс-3 - йодгексен-3 - ов - [9] было установлено, что механизм восстановления радикальный, а не ионный, как при восстановлении 2-фенил - 2-хлорпро-пионовой кислоты. Возможно, здесь влияет местоположение галоида у двойной связи. [4]
При изучении электрохимического поведения ионов цинка и кадмия в органических растворителях уделено большое внимание зависимости механизма и кинетики электродных процессов от природы растворителя и анионного состава раствора. Механизм электродного процесса, в особенности параметры электродной кинетики, в целом определяются следующими факторами: взаимодействие восстанавливающегося иона с растворителем либо ионами фона; взаимодействие между ионами фона и растворителем; положение равновесного потенциала на абсолютной шкале; состав и диэлектрическая проницаемость раствора; распределение восстанавливающихся ионов и ионов фона в двойном слое в начальном и активном состояниях. [5]
 |
Изменение анодного потенция - дет происходить в следующем поряд. [6] |
На основании изучения электрохимического поведения отдельных сульфидов и их сплавов были проведены опыты по анодному растворению указанных выше сульфидных сплавов и заводских штейнов, которые подтвердили возможность анодного растворения сульфидных продуктов с разделением ценных составляющих. [7]
 |
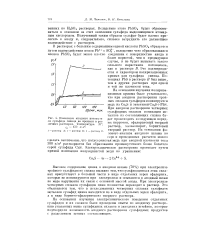
Зависимость потенциалов металлов группы железа от температуры. [8] |
Таким образом, изучение электрохимического поведения никеля, кобальта и железа показало, что в определенной для каждого металла области температур ( выше 100 С) система металл - раствор становится обратимой. Использованный в настоящей работе метод позволяет непосредственно измерять равновесные потенциалы металлов группы железа и на основании полученных данных определять значения равновесных потенциалов этих металлов для различных температур. Приведенные экспериментальные результаты показывают неправильность существующего до сих пор мнения о невозможности определения равновесных потенциалов переходных металлов прямым электрохимическим методом. [9]
Таким образом, изучение электрохимического поведения Ti - 0 2 % Pd в растворах хлоридов при температуре 160 С показало, что сплав обладает высокой коррозионной стойкостью в условиях щели. [10]
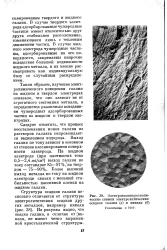 |
Электронномикроскопи-ческие снимки электролитических осадков галлия ( а и никеля ( б. [11] |
Таким образом, изучение электрохимического поведения галлия на жидком и твердом электродах показало, что оно зависит не от агрегатного состояния металла, а определяется различным поведением чужеродных адсорбированных частиц на жидком и твердом электродах. [12]
Основным фундаментальным вопросом при изучении электрохимического поведения полимерных электродов является механизм переноса заряда через слой катализатора. Скорость переноса заряда часто оказывается лимитирующей для электрохимических реакций и каталитических процессов на таких электродах. [13]
Применение метода импульсной поляризации для изучения электрохимического поведения окислов и окисленной поверхности металла. [14]
Следует высказать надежду, что изучение электрохимического поведения различных блескообразователей внесет новые ценные данные в проблему получения блестящих осадков металлов на катоде. [15]
Страницы: 1 2