Изучение - электродный потенциал
Cтраница 1
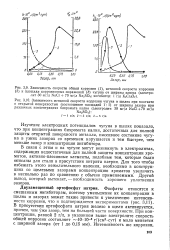
Изучение электродных потенциалов именно и этих условиях может дать важные сведения о коррозионном поведении металла при переменных напряжениях. По величине их можно судить о расположении полюсов при контакте участков, подверженных различным по величине переменным напряжениям, а также об опасности этого контакта в смысле локализации коррозии и о защитных свойствах оксидных пленок, образующихся на поверхности металла, подверженного переменным напряжениям. [1]
Изучение электродных потенциалов чугуна в щелях показало, что при концентрациях бихромата калия, достаточных для полной защиты открытой поверхности металла, пассивное состояние чугуна в узких зазорах со временем нарушается и тем быстрее, чем меньше зазор и концентрация ингибитора. [3]
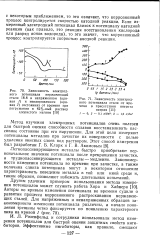
Метод изучения электродных потенциалов очень полезен для быстрой оценки способности сплавов восстанавливать пассивное состояние при его нарушении. Для этой цели измеряют потенциалы металлов при зачистке их поверхности с целью удаления окисных слоев под раствором. [5]
Экспериментальные данные по изучению электродных потенциалов позволяют заключить, что различные алюминиевые сплавы в контакте со сталью будут вести себя неодинаково. Контактная коррозия должна быть более интенсивной на лы из сплавов имеющих более отрицательные электродные по; тенцизлы. Однако для более определенной количественной оценки контактной коррозии необходимо знать не только электродные потенциалы, но и поляризационные характеристики сплавов. [6]
Наиболее объективная оценка относительной активности свободных металлов может быть получена методом изучения электродных потенциалов ( гл. [7]
Наиболее объективная оценка относительной активности свободных - металлов может быть получена методом изучения электродных потенциалов ( гл. [8]
Так как влияние уротропина сильнее всего сказывается на коррозии железа-армко, то последнее было использовано в качестве объекта для изучения электродных потенциалов. В исходном электролите, не содержащем уротропина, потенциал железа в первое время облагораживается ( фиг. [9]
 |
Поляризационная диаграмма коррозионного элемента. [10] |
Таким образом, реакции в гальваническом элементе аналогичны протеканию электрохимических процессов коррозии, которые основываются в основном на изучении общих законов механизма работы коррозионных гальванических элементов, изучении электродных потенциалов и кинетики электродных реакций. [11]
Протекание коррозионного процесса электрохимическим путем, таким образом, аналогично протеканию реакции в гальваническом элементе. Поэтому теория процессов электрохимической коррозии в значительной мере основывается на изучении общих законов механизма работы коррозионных гальванических элементов и, в частности, на изучении электродных потенциалов и кинетики электродных реакций. [12]
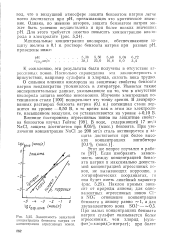 |
Зависимость защитной концентрации бензоата натрия от концентрации агрессивных ионов. [13] |
О сильном влиянии кислорода на защитные свойства бензоата натрия неоднократно упоминалось в литературе. Имеются также экспериментальные данные, указывающие на то, что в отсутствие кислорода защита вообще невозможна. Изучение электродных потенциалов стали [100] подкрепляет эту точку зрения. В, в то время как в этом же электролите, насыщенном воздухом, он устанавливается на уровне 0 10 В. [14]
При исследовании поверхности платиновой черни прогрессивным отравлением ее различными соединениями Мэкстед и его сотрудники s не обнаружили более двух типов активных участков. Определение дифференциальной теплоты адсорбции, проведенное Мэкстедом и Кассидом 6, показало постоянное значение последней в большом интервале покрытия поверхности. К тому же выводу приходят Фрумкин и Щлыгин 8 на основании изучения электродных потенциалов платиновой черни при различном количестве адсорбированного ею водорода. [15]
Страницы: 1 2