Изучение - электродный процесс
Cтраница 1
Изучение электродных процессов потенциокинетическим методом применительно к электрохимической обработке металлов. [1]
Изучение электродных процессов при использовании линейно повышающегося потенциала на растущей ртутной капле производится обычно при столь высоких значениях v, что для наблюдения и регистрации кривых используют катодный осциллограф, при этом сам этот метод исследования часто рассматривают как одну из разновидностей осциллографической полярографии. Если электродный процесс включает в себя две последовательные электрохимические стадии, протекающие при разных потенциалах, или же в растворе присутствуют два деполяризатора, различающиеся по легкости вступления в электрохимическую реакцию, то на осциллополярограммах наблюдается два максимума. Определение / макс второго максимума представляет известные трудности [48], так как для его нахождения из наблюдаемой величины максимального тока необходимо вычесть значение тока, отвечающего первому электродному процессу, которое обычно находится экстраполяцией [49] ниспадающего участка кривой после первого максимума. [2]
Изучение электродных процессов по-тенциокинетическим методом применительно к ЭХО металлов / А. Д. Давыдов, Л. Л. Кноц, В. [3]
Изучение электродных процессов, протекающих при наличии адсорбированных органических веществ, непосредственно связано с исследованием влияния строения двойного слоя. [4]
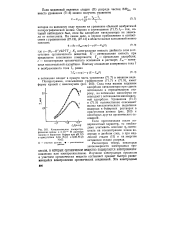 |
Каталитические полярографические волны вЗ - 10 - 6 М растворе хинина в боратном буфере при рН 9 5 в присутствии 0 04 М ( / и 0 06 М ( 2. [5] |
Изучение электродных процессов Q участием органических веществ составляет предмет быстро развивающейся электрохимии органических соединений. [6]
Для изучения электродных процессов, осложненных различного типа промежуточными химическими реакциями, предложены разнообразные электрохимические методы и соотношения между параметрами. Широкое применение при изучении процессов EGE находит хронопотенциометрия. [7]
Методы изучения электродных процессов делятся на классические и релаксационные. Классическими называют методы снятия стационарных поляризационных кривых, основанные на определении зависимости: величина поляризующего тока - стационарное значение потенциала электрода. [8]
При изучении электродных процессов следует помнить, что по-тенциостатический метод имеет ряд принципиальных ограничений. Необходимо учитывать, что измеряемая при каждом потенциале плотность тока - это алгебраическая сумма скоростей всех возможных при этом потенциале анодных и катодных реакций. Поэтому токовые поляризационные кривые указывают на зависимость скорости растворения или катодного восстановлшия окисленных частиц раствора от потенциала только в том случае, когда скорости возможных при данном потенциале посторонних катодных или анодных реакций неизмеримо меньше, чем скорости исследуемых реакций. Эти условия не выполняются при потенциалах, близких к потенциалам саморастворения. [9]
При изучении электродных процессов некоторые авторы приписывают ультразвуку специфический эффект в явлениях адсорбции. С помощью радиоактивных изотопов установлена степень десорбции, вызываемой ультразвуковым полем. [10]
При изучении электродных процессов с участием органических веществ необходимо учитывать возможность образования свободных радикалов в качестве промежуточных продуктов реакции. Радикалы обнаружены при электровосстановлении ненасыщенных углеводородов, хинонов, карбонильных и нитросоединений и других классов органических веществ на ртути и других металлах. Образование радикалов происходит и при реакциях электроокисления. [11]
При хронопотенциометрическом изучении электродных процессов с приэлектродными химическими реакциями переходное время Тк определяется константами скорости прямой и обратной химических реакций р ира. [12]
При хронопотенциометрическом изучении электродных процессов с приэлектродными химическими реакциями переходное время tfc определяется константами скорости прямой и обратной химических реакций р ира. [13]
При хронопотенциометрическом изучении электродных процессов с приэлектродными химическими реакциями переходное время определяется константами скоростей прямой и обратной химических реакций. Применение хронопотенциометрического метода для изучения химических реакций, предшествующих переносу электрона, позволяет определять скорости реакций почти на два порядка более высокие, чем те, которые можно определить методами полярографии. [14]
Большое значение для изучения электродных процессов имеет хронопотенциометрия с изменением направления поляризации при достижении переходного времени. Делахей [239], позволяет одновременно изучать и катодные и анодные процессы. Если обращение поляризации происходит без изменения плотности тока, то переходное время обратного процесса составляет J / 3 от переходного времени прямого процесса. [15]
Страницы: 1 2 3 4