Изучение - равновесие - жидкость-пары
Cтраница 1
Изучение равновесия жидкость-пар на модельных системах показало, что разделяющие свойства нефтяных сульфонов и сульфоксидов обусловлены резким снижением коэффициентов активности сероорганических соединений ( меркаптанов, сульфидов, дисульфидов, тиофенов) в присутствии растворителя. Селективные свойства изученных растворителей остаются высокими вплоть дократности сырья к растворителю 1: 1 - 1: 2 при высокой растворяющей способности. [1]
Изучение равновесия жидкость-пар в двойных системах, образованных изопропил-аминами, водой и изопропаном, Отч. [2]
Методы изучения равновесий жидкость-пар обстоятельно описаны в литературе. [3]
Целью данной работы явилось изучение равновесия жидкость-пар в системах: акриловая кислота-уксусная кислота-вода, акриловая кислота-уксусная кислота - - гептап п акриловая кислота-уксусная кислота-четыреххлористый углерод. [4]
С этой целью сконструирована усовершенствованная проточная установка для изучения равновесия жидкость-пар. С помощью этой установки получены данные для смесей углеводородов с метилпирролидоном. Данные согласуются с вычислениями, проведенными по теории Ренона-Праусница, показывая ее применимость для изученных смесей. [5]
 |
Прибор Бушмакина. [6] |
Настоящая глава не претендует на полный обзор методов изучения равновесий жидкость-пар и, тем более, конструкций, предложенных для решения этой задачи приборов и установок. Авторы стремились отразить основные тенденции и достижения в развитии методов эксперимента за последние десятилетия и привести некоторые сведения по экспериментальному изучению равновесийЦжид - кость-пар и жидкость-жидкость-пар в ЛГУ. [7]
Из причин, порождающих систематические ошибки, при изучении равновесий жидкость-пар на первое место следует поставить недостаточную чистоту реактивов. Небольшие примеси, даже до 1 %, особенно примеси легколетучего компонента, могут приводить к существенным ошибкам. В то же время при загрязненном реактиве результаты измерений обладают хорошей воспроизводимостью, что создает ложное впечатление о высокой точности данных. [8]
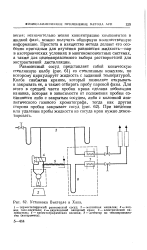 |
Установка Вихтерле и Хала. [9] |
Простота и изящество метода делают его особенно пригодным для изучения равновесия жидкость-пар в изотермических условиях в многокомпонентных системах, а также для целенаправленного выбора растворителей для экстрактивной дистилляции. [10]
 |
Установка Дитриха. [11] |
В отличие от обычных методов, которые в процессе изучения равновесия жидкость-пар при пониженных давлениях позволяют получить лишь приближенные величины, прибор, разработанный Дитрихом ( рис. 63), дает удовлетворительные результаты и при этих пониженных давлениях. В данном методе давление непосредственно не измеряется, а рассчитывается по методу Вихтерле и Хала, что позволяет обойтись без обезгаживания жидкой смеси. Состав смеси задается просто путем смешивания известных весовых количеств двух чистых жидкостей. В процессе установления равновесия жидкость необходимо непрерывно перемешивать. [12]
Авторы [74] указывают тот объем работы, который необходим при изучении равновесия жидкость-пар методом открытого испарения. Например, для исследования неазеотропной двойной системы оказывается достаточно одного опыта, поскольку исходный раствор можно подобрать всегда так, чтобы его состав в ходе испарения прошел необходимый концентрационный интервал. Для сравнительно полного исследования равновесия жидкость - пар в тройной системе требуется поставить 3 - 5 опытов по испарению. Это примерно соответствует при обычных методиках исследованию фазовых равновесий по 3 - 5 секущим концентрационного треугольника. В четверной системе ( ацетон-бензол-толуол - циклогексан) потребовалось 16 опытов, причем на проведение исследования было израсходовано не более 50 г каждого компонента. [13]
Поэтому полная несмешиваемость, которая редко встречается даже в первом приближении при изучении равновесий жидкость-пар, наблюдается по меньшей мере в первом приближении в большинстве равновесий кристаллическая фаза - жидкость. [14]
Страницы: 1