Изучение - равновесие - реакция
Cтраница 3
На рис. 16 изображена схема установки для изучения равновесия реакции, когда исходными веществами в реакции являются окись углерода и водяной пар. [31]
На рис. 53 изображена схема установки для изучения равновесия реакции. В качестве электролита применяют 17 % - ный раствор едкого натра. Электролиз ведут на никелевых электродах. [32]
Между индикаторными реакциями, применяемыми для анализа и изучения равновесий реакций комплексообразования, существует известное сходство. [33]
Задачей настоящей работы является получение указанных данных путем изучения равновесия реакций ниобия и тантала с кислородом и азотом при очень высоких температурах. [34]
По этим причинам сравнение устойчивости карбоний-ионов по данным изучения равновесия реакции протонирования в кислых растворах может быть сделано с такой же степенью достоверности, как и для случая ионизации спиртов, лишь при определении соответствующей функции кислотности, применимой к данным замещенным углеводородам. [35]
На рис. 14 отдельно изображено устройство контактного узла установки для изучения равновесия реакции. В кольцевое пространство между кожухом термопары и внутренней стенкой фарфоровой трубки загружают около 100 см3 смеси, составленной из ванадиевого катализатора и дробленого кристаллического кварца. Перед загрузкой смеси в реакционную трубку катализатор должен быть предварительно обработан двуокисью серы, разбавленной воздухом. [36]
На рис. 14 отдельно изображено устройство контактного узла установки для изучения равновесия реакции. [37]
В последующей работе этого же автора [234] на основании результатов изучения равновесия реакции US La LaS U в газовой фазе масс-спектрометрическим методом при температурах 2207 - 2497 К определена энергия диссоциации LaS, среднее значение которой принято равным 136 3 ккал / моль. Вычислена стандартная теплота образования LaS, равная - 108 4 ккал / моль. [38]
В комплексном ионе [ TIIJ таллий, как это установил Абегг при изучении равновесия реакции, трехвалентен. [39]
Как правило, при использовании кинетических методов анализа определяют равновесную, а не общую концентрацию вещества, поэтому указанные методы с успехом можно применять при изучении равновесий в растворах и, в особенности, при изучении равновесий реакций образования комплексных соединений. [40]
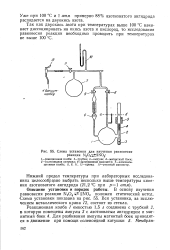 |
Схема установки для изучения равновесия. [41] |
В основу изучения равновесия реакции N2O45 2NO2 положен статический метод. Вся установка, за исключением металлического крана 12, состоит из стекла. [42]
Подробно, хотя и не всегда достаточно строго, обсуждаются колебательные и электронные спектры молекулярных комплексов. Авторы кратко описывают экспериментальные методы изучения равновесия реакций образования я-комплексов и приводят сводку количественных данных, которая служит основой для сопоставления акцепторных и донорных свойств компонентов комплексов, а также используется для некоторых заключений о их строении. [43]
Задача эта была поставлена перед немецкими учеными промышленностью. Тогда вновь были предприняты экспериментальные работы по изучению равновесия реакции. [44]
Значения теплот образования окисей платины и серебра резко различаются, что указывает на неоднородность энергии связи кислорода с поверхностью металлов. Киперман и Баландин [105] определили энергии связи кислорода с никелем при изучении равновесия реакции [ Ni ] 0 На; [ Ni ] - f - Н20 - Энергия связи, полученная этим методом, составляет 57 1 - 59 9 ккал. [45]
Страницы: 1 2 3 4