Изучение - ионообменное равновесие
Cтраница 1
Изучение ионообменного равновесия в системе Н - 1Л показывает, что по всей области составов ионитов преимущественно поглощаемым новом является ион водорода. Интересно отметить что с увеличением эквивалентной доли Li в растворе возрастает эквивалентная доля его в фазе катионита. [1]
Изучение ионообменных равновесий представляет собой одну из основных задач при характеристике ионообменных свойств цеолитов. При этом важное значение имеет правильная интерпретация полученных результатов. [2]
Изучение ионообменного равновесия в органических и кодно-орга-нических средах вызывает определенный интерес исследователей, поскольку подбором соответствующих растворителей можно управлять процессом ионообменной сорбции на одном и том же образце смолы, что значительно расширяет область практического применения ионитов. [3]
Изучению ионообменных равновесий катионов щелочноземельных металлов уделялось значительно меньше внимания, чем щелочным. Поэтому нижеприведенные данные в большинстве своем являются оригинальными. [4]
Подобный ряд был получен нами при изучении ионообменных равновесий и с другими вытесняющими катионами. При обмене катионов одинаковой ва-летности влияние температуры в интервале 20 - 70 С не оказывает заметного влияния на величину константы равновесия. [6]
Подобный ряд был получен нами при изучении ионообменных равновесий и с другими вытесняющими катионами. При обмене катионов одинаковой ва-летности влияние температуры в интервале 20 - 70 С не оказывает заметного влияния на величину константы равновесия. При обмене ионов разной валентности ( NEtf - Саг, Na - Са2) повышение температуры вызывает изменение константы обмена. [7]
Подобный ряд был получен нами при изучении ионообменных равновесий и с другими вытесняющими катионами. При обмене катионов одинаковой ва-летности влияние температуры в интервале 20 - 70 С не оказывает заметного влияния на величину константы равновесия. При обмене ионов разной валентности ( NHJ - Са2, Na - Са2) повышение температуры вызывает изменение константы обмена. [8]
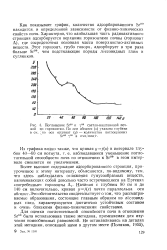 |
Поглощение Sr90 и f30 светло-каштановой почвой по горизонтам. По оси абсцисс ( д - указана глубина в см, 1 по оси ординат ( у - количество поглощаемых. [9] |
Для оценки поглотительной способности почв в отношении Sr90 была использована также методика, применяемая для изучения ионообменных равновесий. [10]
В последние годы отмечается значительный интерес к использованию стеклянных электродов в расплавленных солях. Однако рациональное применение их требует изучения ионообменных равновесий на границе стекло-расплавленный электролит и выяснения взаимосвязи между ионообменными процессами и структурой электродного стекла. Одним на важных аспектов изучения электродного поведения стекла является и проблема специфичности основной функции стеклянного электрода в присутствии других ионов металлов, как одно -, так и двухзарядных. В этом плане и развиваются исследования в лаборатории электрохимии стекла ЛГУ. [11]
Равновесия, устанавливающиеся при ионообменных процессах, являются предметом многочисленных исследований; из первых работ, выполненных на почвах и на других разнообразных, случайно выбранных материалах, нужно в первую очередь упомянуть исследования Ганса, проведенные на синтетическом плавленом цеолите ( пермутит натрия фирмы Permutit-AG), и обстоятельные работы Ротмунд-Корнфельд, Дженни и др. на об-менниках аналогичного типа. Затем следует назвать многочисленные, тщательно выполненные исследования на минеральных ионообменниках - цеолитах, бентонитах, природных и стабилизированных глинах ( Маршалл и Гупта, Меллер, Шахтшабель и др.), а также изучение ионообменных равновесий на сульфитной целлюлозе ( дю Ритц), крахмале, белке, казеине ( Граф) и других органических веществах. [12]
Страницы: 1
