Изучение - разложение
Cтраница 1
Изучение разложения в ряд Фурье вблизи точки разрыва. [1]
Изучение разложения КМГП при температурах, при которых разложение еще не проявляется ( 60 С), и в присутствии солей кобальта ( II) показало, что это реакция первого порядка [251], не зависящая от концентрации КМГП. Растворитель же влияет на скорость. [2]
 |
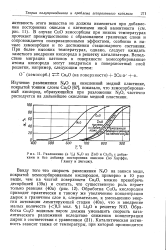
Влияние концентрации хлористого водорода на разложение бутилнитрита. Температура 20 С, растворитель - бута-нол, . ( C4H9ONO 0 02 моль / л. [3] |
Изучение разложения адкщшитритов в интервале концентраций хлористого водорода ( рис. 2) показало, что реакция подчиняется закономерностям кислотного катализа. [4]
Изучение разложения полимеров под действием высокой температуры в отсутствие кислорода воздуха ( обычно в вакууме) и в окислительной атмосфере, а также определение влияния ультрафиолетового облучения позволяет установить характер, а часто и механизм протекающих процессов. Это дает возможность более обоснованно подойти к выбору соответствующих стабилизаторов. Такие испытания, однако, не всегда выполнимы, поскольку работы по изучению разложения полимеров сравнительно трудоемки и требуют специального оборудования. Кроме того, методы - подобных исследований пока еще не стандартизованы. Поэтому во многих случаях на практике приходится ограничиваться проведением испытаний материалов с учетом их возможной переработки и последующего воздействия повышенной температуры, а также солнечного света. [5]
 |
Разложение ( в / 0 N2O на ZnO и Сг2О3 с добавками и без добавки посторонних окислов ( по Хауффе, Глангу и Энгелю. [6] |
Изучение разложения NaO на окисленной медной пластинке, покрытой тонким слоем Си2О [67], показало, что хемосорбирован-ный кислород, образующийся при разложении N2O, частично расходуется на дальнейшее окисление медной пластинки. [7]
Изучение разложения перекиси ацетила в растворе изооктана подтверждает эти выводы. Выход двуокиси углерода на моль разложившейся перекиси составляет 1 81 для 1 3 - 10 - 3 М раствора перекиси. Это отношение не меняется при добавке таких радикальных ловушек, как иод, хинон или стирол. Недостаточное количество образующейся двуокиси углерода означает, что выход метилацетата составляет 20 %; так как его выход не зависит от наличия радикальных ловушек, снова можно заключить, что он всецело образуется в результате клеточного или радикального процесса. [8]
Изучение разложения изопропилового спирта в адсорбированном слое на различных окислах [237] показало, что активные центры дегидрирования отличны от активных центров дегидратации. Поэтому избирательность в реакции разложения спиртов обусловлена относительной активностью катализатора в двух основных реакциях: дегидрировании и дегидратации, которые протекают независимо. Шкала каталитических активностей в табл. 3 подобрана таким образом, чтобы ( хотя и весьма приближенно) можно было судить, какая из этих реакций преобладает на данном катализаторе. [9]
Изучение разложения перекиси бария ( 96 5 % Ва02) в кислороде, воздухе, азоте при разных концентрациях влаги ( от 0 до 0 018 г / л) в интервале 300 - 600 С показало, что процесс окисления гидроокиси бария должен идти с максимальной скоростью при температурах 550 - 600 С. Именно при этих температурах чувствительность перекиси бария к влаге минимальна, а следовательно, минимальной может быть и подача кислорода. [10]
Изучение разложения сернистого бария хлористым магнием, Отч. [11]
Изучение разложения метилового спирта с помощью катализатора, состоящего из смеси оксидов цинка и хрома, выявило зависимость этого процесса от предварительной обработки оксидов давлением. [12]
Для изучения разложения щавелевой кислоты в концентрированы эй серной кислоте при 323 К приготовили 1 / 40 М раствор щавелевой кислоты в 99 5 % - ной серной кислоте. [13]
При изучении разложений некоторого элемента с некоммутативного кольца R удобно рассматривать модуль R / cR, свойства которого отражают все свойства разложений этого элемента. [14]
При изучении разложения гидразина было установлено, что промежуточные радикалы могут взаимодействовать друг с другом с образованием молекулы гидразина. Такие радикалы могут выделяться не только при разложении гидразина, но и аммиака. Это открывает путь получения гидразина через разложение аммиака. [15]
Страницы: 1 2 3 4