Начальный участок - кинетическая кривая
Cтраница 2
Начальный участок кинетической кривой удовлетворительно описывается большинством уравнений, характеризующих нестационарную работу ректификационных колонн. [16]
Первый член правой части уравнения ( 79) выражает скорость реакции при независимом росте ядер, а остальные - поправку на перекрывание ядер. Для начального участка кинетической кривой можно пренебречь всеми членами правой части уравнения, кроме первого, что позволяет определять коэффициент при первом члене в независимых изменениях. Такое определение целесообразно проводить на первой ступени анализа экспериментальных данных. Кроме константы % уравнение ( 79) включает параметры функции распределения а и а. Эти параметры имеют следующий смысл. Параметр а для данной задачи численно равен времени, при котором число касаний ядер в единицу времени максимально. [18]
Первый член правой части уравнения ( 79) выражает скорость реакции при независимом росте ядер, а остальные - поправку на перекрывание ядер. Для начального участка кинетической кривой можно пренебречь всеми членами правой части уравнения, кроме первого, что позволяет определять коэффициент при первом члене в независимых изменениях. Такое определение целесообразно проводить на первой ступени анализа экспериментальных данных. Эти параметры имеют следующий смысл. Параметр а для данной задачи численно равен времени, при котором число касаний ядер в единицу времени максимально. [20]
Моно исследовал зависимость тангенса угла наклона начального участка кинетической кривой роста популяции от начальной концентрации субстрата в питательной среде. Тангенс угла наклона начального участка кинетической кривой по существу и есть максимальная удельная скорость роста популяции. [21]
Отметим, что полученные уравнения неоднократно пытались применять и для описания более сложного случая ионного обмена. Обычно в этом случае ими удовлетворительно описывается некоторый начальный участок кинетической кривой, что, по-видимому, объясняется возможностью достаточно точной аппроксимации начального участка изотермы обмена прямой линией. С другой стороны, весьма часто и в случае сорбции микроколичеств вещества, и в случае изотопного обмена, график [ ln ( l - F) t ] становится прямолинейным лишь спустя некоторое время после начала эксперимента. Возможно, что в таких случаях исследуемый процесс еще находится в смешаннодиффузионной области, а чисто внешнедиффузионная область не достигнута. [22]
Это уравнение также справедливо для описания чисто внешне-диффузионного процесса при линейной изотерме сорбции и постоянно обновляющемся растворе. Так же как и в случае сферического зерна, начальный участок кинетической кривой линеен в координатах F - t и имеет угловой коэффициент 3Bi O / ( l p р2) Z23Z) / ( l p p2) SIKj, а кривая, построенная в координатах F-Jt, имеет S-образную форму. [23]
Сопоставление с экспериментальными данными уравнения (3.50), включающего, как минимум, три независимых параметра, представляет довольно сложную процедуру. В данном случае задача упрощается в связи с тем, что параметр к может быть определен из данных для начального участка кинетической кривой. [24]
Удобным экспериментальным критерием определения режима протекания реакции являются опыты со слоями твердого реагента - возрастающей толщины. До тех пор пока не будет достигнута граничная толщина, скорость реакции, выраженная через степень превращения, не должна зависеть от массы навески. Пренебрежение точной информацией о граничной толщине может привести к серьезным погрешностям не только в определении абсолютной величины скорости реакции, но и в определении энергии активации начального участка кинетической кривой. [25]
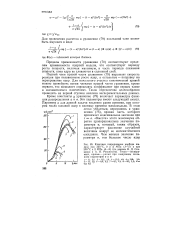
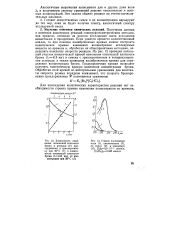
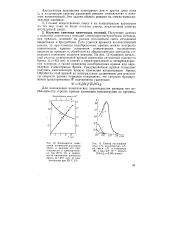
Получение данных о кинетике химических реакций спектрофотометрическим методом, как правило, основано на разном поглощении света исходными веществами и продуктами. Если удается провести количественный анализ, то при помощи калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени и, обработав их общепринятыми методами, определить константу скорости реакции. На рис. 12 приведен начальный участок кинетической кривой изменения оптической плотности брома ( А 415 км) в смесях с трихлорэтиленом в четыреххлорис-том углероде, а также приведена калибровочная кривая для определения концентрации брома. Градуировочная кривая позволяет получить кинетическую кривую изменения концентрации брома. [27]
Получение данных о кинетике химических реакций спектрофотометрическим методом, как правило, основано на разном поглощении света исходными веществами и продуктами. Если удается провести количественный анализ, то при помощи калибровочных кривых можно построить кинетические кривые изменения концентрации исследуемых веществ во времени и, обработав их общепринятыми методами, определить константу скорости реакции. На рис. 12 приведен начальный участок кинетической кривой изменения оптической плотности брома ( Я415 км) в смесях с трихлорэтиленом в четыреххлорис-том углероде, а также приведена калибровочная кривая для определения концентрации брома. Градуировочная кривая позволяет получить кинетическую кривую изменения концентрации брома. [29]
Измеряют, как указывалось выше, зависимость скорости реакции от начальной концентрации реагента. Практически определение проводят следующим образом. Как и в первом случае, строят кривую по экспериментальным точкам, но проводят серию экспериментов с различной начальной концентрацией реагента. Далее к начальной точке каждой кривой проводят касательную и определяют наклон. Обычно построение касательных не вызывает затруднений, так как начальный участок кинетической кривой слабо искривлен. Если же кривизна значительна, прибегают к помощи зеркала. Прямоугольное зеркало устанавливают вертикально так, что отражение кривой в зеркале ( в1 заданной точке) является плавным без излома продолжением кривой на рисунке. Это означает, что зеркало установлено строго перпендикулярно касательной, которую следует построить в заданной точке. Вдоль нижней грани зеркала проводят прямую линию, из точки ее пересечения с кривой строят перпендикуляр. Скорость реакции в данной точке рассчитывают как тангенс угла наклона касательной к оси абсцисс с учетом выбранного масштаба координатной сетки. [30]
Страницы: 1 2 3