Учет - неидеальность - паровая фаза
Cтраница 1
Учет неидеальности паровой фазы при давлениях до 2 атм практически не влияет на результаты предсказания, при более высоких давлениях он всегда улучшает результаты, но в большинстве случаев крайне незначительно. [1]
Следовательно, задача учета неидеальности паровой фазы сводится к расчету летучести. Для этого, согласно уравнению ( 40), необходимо знать зависимость между удельным объемом пара и давлением. Поскольку температура, при которой исследуется равновесие, тоже в общем случае является переменной величиной, для точного расчета летучести нужно располагать экспериментальными данными о зависимости Р-V-Т для пара. Способы расчета летучести по существу отличаются друг от друга только использованием различных форм зависимости молярного объема реального газа от давления. [2]
Следовательно, задача учета неидеальности паровой фазы сводится к расчету летучести. Для этого, согласно уравнению ( 40), необходимо знать зависимость между удельным объемом пара и давлением. Поскольку температуря, при которой исследуется равновесие, тоже в общем случае является переменной величиной, для точного расчета летучести нужно располагать экспериментальными данными о зависимости Р - V - Т для пара. Способы расчета летучести по существу отличаются друг от друга только использованием различных форм зависимости молярного объема реального газа от давления. [3]
Следовательно, задача учета неидеальности паровой фазы сводится к расчету летучести. [4]
Таким образом, для учета неидеальности паровой фазы необходимы значения мольных объемов паровой фазы, вторых вири-альных коэффициентов, критических параметров, дипольного момента, ацентрического фактора. [5]
Специально рассматривается возможность применения метода к проверке изобарных данных и необходимость учета неидеальности паровой фазы. Показывается на основе общего анализа этих методов и привлечения большого объема экспериментального материала по теплотам смешения жидкостей и вторым вириальным коэффициентам паров, что метод может быть широко использован для проверки изобарных данных и что в большинстве случаев нет необходимости в учете неидеальности паровой фазы. Последние заключения относятся как к предлагаемому методу, так и к методу Редлиха - Кистера. [6]
В системах окись пропилена - изопррпанол, метил формиат - окись пропилена учет неидеальности паровой фазы не приводит к улучшению описания парожидкостного равновесия. Сравнение коэффициентов активности компонентов, рассчитанных в предположении идеальности и неидеальности паровой фазы показывает, что расхождение между ними не. В связи с этим расчеты парожидкостного равновесия в бинарных, тройных и четырехком-гюнентных системах, приведенные в статье, сделаны для идеальной па-ррвой фазы. [7]
В зависимости От исходных данных о физико-химических свойствах компонентов, а также данных по парожидкостному равновесию бинарных и многокомпонентных смесей возможно несколько вариантов расчета равновесия: 1) при допущении постоянства коэффициентов относительной летучести компонентов; 2) с учетом температурной зависимости констант фазового равновесия при допущении идеальности паровой и жидкой фаз; 3) с учетом неидеальной жидкой фазы по уравнениям Маргулеса, Ван Лаара, Редлиха - Кистера, Вильсона; 4) с учетом неидеальности паровой фазы через вириальное уравнение состояния. [8]
В зависимости от исходных Данных о физико-химических свойствах компонентов, а также данных по парожидкостному равновесию бинарных и многокомпонентных смесей возможно несколько вариантов расчета равновесия: 1) при допущении постоянства коэффициентов относительной летучести компонентов; 2) с учетом температурной зависимости констант фазового равновесия при допущении идеальности паровой и жидкой фаз; 3) с учетом неидеальной жидкой фазы по уравнениям Маргулеса, Ван Лаара, Редлиха - Кистера, Вильсона; 4) с учетом неидеальности паровой фазы через вириальное уравнение состояния. [9]
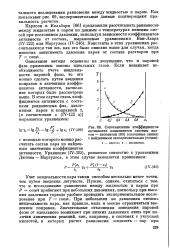 |
Сопоставление коэффициентов активности компонентов системы ацетон - изопентан ( сплошные линии с найденными экспериментально ( точки. [10] |
Описанные методы основаны на допущении, что к паровой фазе применимы законы идеальных газов. Если возникает необходимость учета неидеальности паровой фазы, то это можно сделать путем введения поправок к значениям коэффициентов активности, вычисление которых было рассмотрено выше. [11]
Результаты расчетов для бинарных систем бензол - циклогексан, метиловый спирт - четыреххлористый углерод, ацетон - гептан и ацетон - хлороформ подтверждают приведенную выше общую оценку величин In у, A In - у и A In у. Это означает, что для учета неидеальности паровой фазы при расчете коэффициентов активности необходимо иметь данные о вторых вириальных коэффициентах не только для индивидуальных веществ, но и для смеси. Если же учитывать только коэффициенты B ( i, то вычисленные значения коэффициентов активности могут отличаться от истинных даже больше, чем рассчитанные в предположении об идеальности пара. [12]
Скет-чардом с сотрудниками [1,44] на основании своих данных 6 равйовесии жидкость-пар, имеют место значительные расхождения между калориметрическими и расчетными значениями теплот смешения. Исходные данные о равновесии можно считать достаточно точными, но учет неидеальности паровой фазы был сделан очень грубо. При расчете значений In - f / вводилась только одна поправка Д In - ff, для определения которой использовались величины вторых вириальных коэффициентов, рассчитанные теоретически по уравнению Кейса. Эти значения Вц для этилового и метилового спиртов и хлороформа сильно отличаются от полученных позднее экспериментально величин вторых вириальных коэффициентов. [13]
В литературе предложено большое число уравнений, определяющих зависимость давления насыщенного пара от температуры. Эти уравнения, как правило, являются видоизменениями уравнения Клаузиуса - Клапейрона, отличаются способом интегрирования, разными приемами учета неидеальности паровой фазы. [14]
Иное положение наблюдается в системах, состоящих из неполярных ( нормальных) веществ, подчиняющихся закону соответственных состояний. Для таких систем, как уже указывалось выше, вторая поправка близка к нулю и для расчета коэффициентов активности с учетом неидеальности паровой фазы достаточно иметь значения вторых вириальных коэффициентов чистых веществ. [15]
Страницы: 1 2