Учет - влияние - среда
Cтраница 3
Реакции ароматических соединений обычно проводят в жид - кой фазе в среде растворителя, роль которого может играть одно из реагирующих веществ. Молекулы растворителя взаимодействуют с реагирующими частицами на всех этапах реакции, образуя вокруг них сольватные оболочки, которые могут изменять свободную энергию и электронную структуру частиц и, как следствие, скорость, механизм и направление реакции. Без учета влияния среды правильное понимание течения реакций невозможно. [31]
За исключением отдельных газофазных процессов реакции ароматических соединений проводятся в жидкой фазе, в среде растворителя, роль которого может играть одно из реагирующих веществ. Фактически в реакции участвуют не изолированные частицы, которые изображают при написании химических уравнений, а качественно отличные от них сольватные-комплексы. Без учета влияния среды правильное понимание течения реакций невозможно. [32]
Эти явления обязаны, напр. Система ( 23) - ( 25) обладает полнотой, позволяя. V, если для них заданы необходимые начальные и граничные условия; для учета влияния среды вне рассматриваемой области V на процессы внутри нее на ее границе Z требуется ставить нелокальные, интегральные условия. [33]
Реакция металла на эти факторы не однозначна, она связана со степенью охрупчивания материала и склонностью его к растрескиванию в данной среде. Если охрупчивание не имеет места ( например, при общей коррозии во многих природных средах), то существенного изменения реакции не произойдет. В этом случае подход к оценке влияния отмеченных факторов напряженного состояния аналогичен обычному без учета влияния среды. В средах же, вызывающих охрупчивание и растрескивание, последние необходимо учитывать в расчетах. [34]
Возвращаясь к анализу различий в развитии органических и неорганических форм, необходимо подчеркнуть, что для первых влияние среды не всегда является определяющим фактором. Для неорганических форм среда всегда оказывается решающим фактором. Поэтому задача анализа закономерностей отбора в таких совокупностях, как совокупности кристаллов, значительно упрощается, так как требует в первую очередь учета влияния среды. [35]
Зависимость процесса разрыва тс-связи олефина и формирование новой ионной пары, параметры которой близки к исходной, дают основание полагать, что присоединение следующей молекулы олефина к вновь образовавшемуся АЦ протекает по аналогичной схеме. Как и инициирование с помощью слабокислых комплексных катализаторов, рост цепи носит характер согласованного взаимодействия компонентов системы. Сказанное выше, вероятно, справедливо и для реакции олефинов с сольватноразделенными ионными парами типа [ AlC - OH ] С5 ( СН3) 3, т.е. при учете влияния среды. [36]
Зависимость процессов разрыва л-связи олефина и формирование новой ионной пары, параметры которой близки к исходной, дают основание полагать, что присоединение следующей молекулы олефина к вновь образовавшемуся АЦ протекает по аналогичной схеме. Как и инициирование с помощью слабокислых комплексных катализаторов, рост цепи носит характер согласованного взаимодействия компонентов системы. Сказанное выше, вероятно, справедливо и для реакции олефинов с сольватноразделенными люнными парами типа [ А1С13 - ОН ] 8 - С6 ( СН3) 3, т.е. при учете влияния среды. [37]
Опыт показывает, что если одни и те же заряженные тела при неизменном расстоянии между ними помещать в вакууме и в другой какой-либо изолирующей среде, например в воде, то силы взаимодействия между ними будут различны. Из этого следует сделать вывод, что на величину силы взаимодействия между заряженными телами оказывает влияние и среда, в которой находятся эти тела. Для учета влияния среды и введена величина, которую называют диэлектрической проницаемостью среды. [38]
Приведенное выражение константы скорости элементарной реакции в жидкой фазе в принципе решает вопрос о влиянии среды на скорость реакции. Для этого необходимо знать значения коэффициентов активности реагирующих частиц и активированного комплекса, что вызывает большие трудности в их определении. Для активированного комплекса как состояния реакционной системы в наивысшей точке энергетического барьера вдоль координаты реакции ( см. рис. 3.1) коэффициент активности У экспериментально определить практически невозможно. Поэтому при учете влияния среды на скорость жидкофазных реакций приходится пользоваться различными полуэмпирическими и эмпирическими уравнениями и упрощенными моделями активированного комплекса. [39]
Первый связан с тем, что подобное состояние достаточно корректно можно описать лишь в рамках многоконфигурационного расчета, проведение которого встречается с существенными трудностями даже для сравнительно малых молекул. С использованием полуэмпириче-ских ССП подходов ( MINDO / 2, CNDO / FK они показа - ли, что на потенциальной гиперповерхности системы бензол / Н4 - ( а также пиррол / Н и л-ксилол / Н) существует только один минимум, соответствующий структуре а-комплекса ( см. рис. 2.1 а), наиболее устойчивый по энергии я-комплекс ( см. рис. 2.1, б) не является локальным минимумом и может рассматриваться только как переходное состояние ( седловая точка) для реакций 1 2-лротонного обмена в ароматических соединениях. Более детальное рассмотрение потенциальной гиперповерхности системы бензол / Н, предпринятое в работе [47], привело к обнаружению неглубокого ( ж2 5 кДж / моль) локального минимума, примерно соответствующего по структуре дьюаровскому я-комплек-су [22], однако дальнейшие исследования показали что при повышении точности оптимизации гео. Таким образом, прямые квантавохи-мические расчеты, проведенные без учета влияния среды, не подтвердили наличие какого-либо еще промежуточного соединения, кроме а-комплекса, в реакциях ароматического электрофильного замещения. [40]
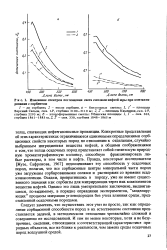 |
Изменение спектров поглощения света смолами нефтей юры при контактировании с сорбентом. [41] |
Конкретные представления об этих характеристиках ограничиваются единичными определениями сорб-ционных свойств некоторых пород по отношению к отдельным, случайно выбранным ингредиентам вещества нефтей, и общими соображениями о том, что толща осадочных пород представляет собой гигантскую природную хроматографическую колонку, способную фракционировать любые растворы, в том числе и нефть. Правда, некоторые исследователи [ Жузе, Сафронова, 1967 ] недооценивают эту способность у осадочных пород, полагая, что все сорбционные центры минеральной части пород уже загружены сорбированными солями и растворами со времени осад-конакопления. Осадки, превратившись в породу, уже не имеют существенного значения как сорбенты для мигрирующих через них компонентов вещества нефтей. Однако это лишь умозрительное заключение, выдвигавшееся, по-видимому, в порядке оправдания экспериментов, моделирующих процессы миграции углеводородов без учета влияния среды, представленной осадочными породами. [42]
Хотя многие данные являются пока неполными и лишь намечают Пути дальнейших исследований, видно, каким мощным средством анализа реакционной способности является рассмотренный метод. Многое еще ждет дальнейших усовершенствований. Недавно разработанные эффективные алгоритмы поиска переходных состояний только начинают внедряться в практику квантовохими-ческих расчетов. Проблемой является учет влияния среды и, в частности, растворителя. [43]
Страницы: 1 2 3