Количественный учет - влияние - растворитель
Cтраница 1
Количественный учет влияния растворителя основывается на рассмотрении работы цикла [1, 3, 19], состоящего из переноса вещества К А из среды М в вакуум, диссоциации КА на ионы К и А - и их сольватации при переносе из вакуума в данную среду. [1]
Количественный учет влияния растворителей упростился бы, если и в этом случае оказалось бы возможным выделить некоторое свойство, присущее большинству или всем растворителям, ответственное за взаимодействие с растворенным веществом. Особенно важно было бы отыскать при этом такие примеры, когда это свойство выступало бы в качестве основы для однородного взаимодействия. [2]
Методы количественного учета влияния растворителя на скорость реакции, основанные на использовании электростатических моделей, неприменимы, если в качестве реагентов выступают неполярные молекулы, сольватация которых в растворе осуществляется в основном за счет дисперсионных сил. Регулярные растворы характеризуются беспорядочным распределением молекул растворителя и растворенного вещества, таким же, как в идеальном растворе. [3]
Необходимо отметить, что строгий количественный учет влияния растворителей на ЕЧ, [ по уравнениям типа ( 126), ( 127) или др. ] невозможен, так как неизвестно изменение скачка потенциала жидкостного соединения при изменении природы растворителя и сохранении неизменным растворителя в электроде сравнения. [4]
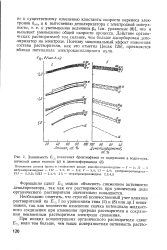 |
Зависимость Ег различных бромтиофенов от содержания в водно-орга. нической смеси этанола ( а и диметилформамида ( б. [5] |
Необходимо отметить, что строгий количественный учет влияния растворителей на Ег 2 [ по уравнениям типа ( 2) и ( 8) или др. ] невозможен, так как неизвестно изменение скачка потенциала жидкостного соединения при изменении природы растворителя и сохранении неизменным растворителя электрода сравнения. [6]
Таким образом, проблема количественного учета влияния растворителя на константу скорости реакции сводится в рамках теории активированного комплекса к определению ( расчетному или экспериментальному) теплот, энтропии и свободных энергий сольватации или коэффициентов активности исходных реагентов и активированного комплекса. Наиболее сложна, конечно, задача определения характеристик активированного комплекса. [7]
 |
Характер изменения концентрации радикалов во времени в реакциях алкоголиза Ph3CCl под действием трет-бутилат-аниона ( а и 2, 4, 6-три-грег - бутилфенолят-аниона ( б. [8] |
Следует, вероятно, предполагать, что в зависимости от условий одна и та же реакция может протекать по типичному гетеролитическому механизму и стадийно, включая перенос одного электрона от донора к акцептору. Это обстоятельство не вносит принципиально новых проблем в количественном учете влияния растворителя. [9]
Не вызывает сомнения, что этот вопрос крайне сложен и в настоящее время не может быть окончательно разрешен, а имеющийся в литературе материал очень ограничен. Исходя из представлений о возможных типах взаимодействия растворенных частиц со средой и используя литературные данные, постараемся по крайней мере выяснить, какие основные сложности возникают при количественном учете влияния растворителя на а-константы заместителей и какие успехи достигнуты в этой области. [10]
Книга посвящена реакциям распада молекул на свободные радикалы, радикальным реакциям замещения, присоединения и распада, реакциям радикалов друг с другом и ионным реакциям с переходом электрона. В работе собрано и систематизировано примерно 8 тысяч констант скоростей элементарных химических реакций, описаны методы намерения констант скоростей молекулярных, радикальных в ионных реакций, рассмотрены вопросы количественного учета влияния растворителя, заместителей и давления на элементарные химические акты. [11]
Страницы: 1