Возникновение - электродный потенциал
Cтраница 2
Причины возникновения электродного потенциала могут быть различными. Так, например, в случае погружения цинковой пластинки в раствор соли цинка, полярные молекулы воды, действуя своими отрицательными полюсами на положительные ионы металла, переводят их в раствор. При этом электроны остаются на поверхности металла, заряжая ее отрицательно. Гидратированные ионы металла, перешедшие в раствор, притягиваются заряженной поверхностью пластинки и располагаются вблизи нее. В результате образуются два слоя с противоположными зарядами - так называемый двойной электрический слой. Процесс перехода ионов металла в жидкость является процессом обратимым. [16]
Механизм возникновения электродного потенциала на границе раздела металл-раствор до настоящего времени является еще недостаточно выясненным. [17]
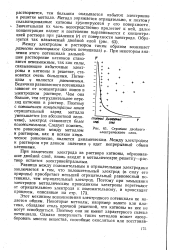 |
Строение двойного электрического слоя. [18] |
Этот механизм возникновения электродного потенциала не является общим. Некоторые металлы, например золото или платина, обладают столь прочной решеткой, что катионы из нее не могут освободиться. Поэтому они не имеют характерного скачка потенциала. [19]
Описанный механизм возникновения электродного потенциала не является общим. Некоторые металлы ( золото, платина) обладают столь прочной кристаллической решеткой, что катионы из нее не могут освободиться. У этих металлов характерный скачок потенциала не возникает. Однако поверхность таких металлов может адсорбировать многие вещества, способные окисляться или восстанавливаться. Поэтому с помощью и этих металлов можно образовать системы, находящиеся в равновесии с растворами. [20]
Кроме явления возникновения электродных потенциалов, при электролизе на электродах имеет место явление перенапряжения. [21]
Согласно Кларку [45], возникновение электродного потенциала обусловлено непосредственным обменом электронами между окислителем и восстановителем. [22]
Согласно этим соображениям процесс возникновения электродного потенциала начинается с диссоциации атомов металла ( внутри самого металла) на ионы и электроны. [23]
Теоретические основы ионометрии ( механизм возникновения электродного потенциала и мембранного транспорта, проблемы селективности и динамические факторы) для стационарных условий эксплуатации электродов разработаны довольно подробно, а теория потенциометрического детектирования в гидродинамических контролируемых условиях стала интенсивно развиваться лишь в последние годы. [24]
Он полагал, что при возникновении электродного потенциала решающее значение имеют следующие два процесса. [25]
Он полагал, что при возникновении электродного потенциала решающее значение имеют два процесса. [26]
Выше уже указывалось, что механизм возникновения электродного потенциала, предложенный Нернстом, хотя и приводит к правильной термодинамически формуле, но не отвечает действительному положению вещей. В последнее время предложен ряд иных попыток объяснения этого механизма. [27]
Пока не будет разработана строгая теория возникновения электродных потенциалов, - основанная на глубоком знании связей между строением металлов, природой электролитных растворов и структурой пограничного слоя, единственным свободным от натяжек путем вывода формулы электродных потенциалов остается чисто термодинамический путь, свободный от всяких гипотез и допущений, но, разумеется, не дающий никакой картины явления. [28]
Выведенное нами уравнение есть основное уравнение осмотической теории возникновения электродных потенциалов. [29]
 |
Двойной электрический слой на границе металл - жидкость ( диффузное строение слоя. [30] |
Страницы: 1 2 3 4