Твердая фаза - вода
Cтраница 1
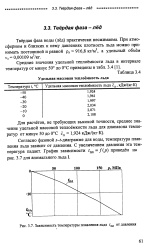 |
Удельная массовая теплоемкость льда.| Зависимость температуры плавления льда tm от давления. [1] |
Твердая фаза воды ( лед) практически несжимаема. [2]
Твердая фаза воды - лед, оказывается, тоже имеет далеко не единственную форму существования. В зависимости от внешних параметров - температуры и давления - реализуется одна из одиннадцати модификаций льда: I / г, 1с, II, III, IV, V, VI, VII, VIII, IX или аморфный лед ( рис. 44), различающихся взаимным расположением молекул воды в решетке кристалла. [3]
 |
Залегание подмерзлотных аллювиальных вод в долине меридионального простирания. [4] |
Для подмерзлотных вод характерно отсутствие твердой фазы воды - льда. Обычно эти воды обладают напором и при вскрытии скважинами часто фонтанируют. По характеру залегания и условиям циркуляции они не отличаются от подземных вод вне-мерзлотных районов, но условия их питания и стока значительно менее благоприятны. [5]
Одной из наиболее замечательных особенностей твердой фазы воды ( льда I) является существование трехмерной сетки водородных связей. Соединенные в жесткий каркас водородными связями молекулы воды образуют единое молекулярное образование - - полимерную молекулу. Каркас льда I содержит полости достаточного размера, чтобы вместить другие молекулы воды. Эти особенности сохраняются в известной степени и в жидком состоянии. Процесс плавления льда связан с нарушением целостности каркаса вследствие усиления теплового движения молекул в жидком состоянии. [6]
Несмотря на то, что возможность перемены погоды при введении твердой фазы воды в переохлажденные облака была ясно продемонстрирована в лаборатории и даже в свободной атмосфере, не было убедительно доказано, что можно систематически изменять количество осадков, выпадающих на поверхность Земли. Трудоемкие эксперименты, основанные на сложных статистических предпосылках, проводились в течение многих лет с большими затратами, но методы, используемые для измерения параметров атмосферы и количества осадков, не могут представить положительный, статистически приемлемый эффект. Таким образом, несмотря на то, что при рассмотрении сложных физических факторов совершенно ясно, что человечество могло бы изменить режим выпадения осадков в достаточно узких пределах, убедительных доказательств этого нет. [7]
Одним из сложных вопросов в этом отношении является природа исходного процесса возникновения зародышей жидкой или твердой фазы воды на поверхности веществ, инородных для воды. В этом случае, например, безоговорочное принятие в расчет констант фазовых переходов воды, а также и других характеристик, относящихся к установлению или разрыву связей между молекулами Н2О, было бы несправедливым, поскольку здесь речь может идти о взаимодействии молекул, не себе подобных, а с молекулами других веществ. Если же, как это нередко делается, рассмотрение начинается с допущения о существовании некоего установившегося слоя молекул воды на инородной поверхности, то тогда речь идет не об образовании зародыша капелек или льдинок, а об их росте. [8]
При дальнейшем понижении температуры этот сигнал быстро исчезает, очевидно, вследствие резкого расширения его при образовании твердой фазы межслоевой воды. С повышением температуры узкий сигнал ЯМР не восстанавливался даже при выдерживании образца при - 2 в течение 5 мин, и только при 0 появлялся спектр, характерный для данного образца при обычных условиях. [9]
Справа от кривой CAD располагается область газообразной фазы воды; между кривыми АВ и AD - область жидкой фазы воды; слева от кривой CAB - область твердой фазы воды. [10]
Вода в твердом состоянии ( кристаллики, прослойки и линзы льда) встречается в горных породах в области многолетней мерзлоты. Вне этой области верхний слой, промерзающий в холодный период, называют сезонной мерзлотой или зимним промерзанием ( подробнее о твердой фазе воды в пластах горных пород сказано в гл. [11]
При равновесии активность вещества в твердой фазе равна его активности в жидкой фазе. Твердая фаза воды ( лед) находится в равновесии с чистой водой при температуре О С. Если лед граничит с раствором, в котором активность растворителя меньше, то равновесие в этом случае наступит при какой-то более низкой температуре. При температуре замерзания чистого растворителя из этого раствора не выпадает твердая фаза: она выпадает при более низкой температуре, соответствующей более низкой активности твердой фазы. Вот почему температура выпадения твердой фазы может быть мерилом активности жидкой воды в растворе. [12]
При равновесии активность вещества в твердой фазе равна его активности в жидкой фазе. Твердая фаза воды ( лед) граничит с чистой водой при температуре 0 С. Если лед граничит с раствором, в котором активность растворителя меньше, то равновесие в этом случае наступит при какой-то более низкой температуре. При температуре замерзания чистого растворителя из этого раствора твердая фаза не выпадает: она выпадает при более низкой температуре, соответствующей более низкой активности твердой фазы. [13]
При равновесии активность вещества в твердой фазе равна его активности в жидкой фазе. Твердая фаза воды ( лед) находится в равновесии с чистой водой при температуре О С. Если лед граничит с раствором, в котором активность растворителя меньше, то равновесие в этом случае наступит при какой-то более низкой температуре. При температуре замерзания чистого растворителя из этого раствора не выпадает твердая фаза: она выпадает при более низкой температуре, соответствующей более низкой активности твердой фазы. Вот почему температура выпадения твердой фазы может быть мерилом активности жидкой воды в растворе. [14]
Как известно, одно и то же вещество в зависимости от внешних условий ( температуры, давления, магнитного или электрического поля, приложенного к телу, и так далее), может находиться в разных состояниях, разных фазах. Соответствующий переход называется фазовым переходом. Например, лед ( твердая фаза воды) при температуре ниже нуля, но при достаточном давлении плавится - это означает, что вода из твердой фазы переходит в жидкую. Помимо переходов из твердого в жидкое или из жидкого в газообразное состояние, существует множество самых различных фазовых переходов. [15]
Страницы: 1 2