Равновесная газовая фаза
Cтраница 2
Рассчитывают среднемольную температуру кипения равновесной газовой фазы и сред-певесовой эквивалентный молекулярный вес жидкой фазы W соответственно составам, которые либо даны, либо рассчитаны по константам равновесия, полученным по ориентировочно взятому значению коррелирующего давления. [16]
По графику находим, что равновесная газовая фаза при давлении 1 атм содержит 0 62 мольной доли димера. [17]
В уравнениях ( 22) неидеальность равновесной газовой фазы учитывается не через соответствующие летучести, а через сжимаемость 2СМ, что в определенном смысле удобнее. [18]
Следовательно, при низких давлениях мольный объем равновесной газовой фазы в точке азеотропа ( экстремум на изотерме Р - N2) должен проходить через экстремальное значение, причем с возрастанием давления объем должен уменьшаться. [19]
Заметим, что при Т 0 плотность равновесной газовой фазы обсуждаемого перехода газ жидкость в макроскопическом электронном газе равна нулю. Соответственно этому и плотность диффузной короны на периферии ячейки, рассчитанная с использованием уравнения состояния этой модели при Т 0, также равна нулю ( см. линию 1 на рис. 58 а. Более того, скачкообразный обрыв до нуля на некотором радиусе плотности электронов в приближениях TFC получается не только для электронейтральной ( атомной) ячейки ( рис. 59), но и для неэлектронейтральных ячеек, соответствующих как положительным, так и отрицательным ионам. Примечательно, что в этом последнем случае избыточный электронный заряд прижимается электростатическими силами к месту обрыва электронной плотности, но не к границе ячейки. [21]
В табл. 13 приведен в качестве примера состав равновесной газовой фазы в системе С02 - С-СО в зависимости от температуры. [22]
По сравнению с методом двойной экстракции при анализе равновесной газовой фазы аналогичным методом является метод двойного отбора проб. [23]
Как при жидкостной экстракции, так и при анализе равновесной газовой фазы невозможно определять истинный объем экстракта и газовой фазы соответственно, если объем сосуществующей нелетучей фазы не может быть измерен. VG знать не нужно; единственное требование заключается в том, что отношения ( j) n / () e и УХ / G Д лжны быть одинаковыми при анализе как исходной, так и стандартизованной систем, что может быть обеспечено при сохранении постоянным отношения веса пробы к объему экстрагента или газовой фазы. К сожалению, методы двойной экстракции и двойного отбора проб неприменимы, если абсолютный объем экстракта или газовой фазы не может быть определен [ ср. [24]
При уменьшении содержания MgCl2 в расплаве концентрация хлора в равновесной газовой фазе резко уменьшается. [25]
Применение трубки для отбора проб позволяет осуществлять интересный вариант анализа равновесной газовой фазы, при котором интересующие нас компоненты вымываются в закрытую петлю, соединенную последовательно с трубкой для улавливания. [26]
Гастингс и Нихолсон [577] сравнили вычисленный и экспериментально найденный состав равновесной газовой фазы процесса изомеризации три - и тетраметилбензолов при 300 и 700 К и пришли к выводу, что данные совпадают в пределах, обусловленных возможными ошибками в анализе продуктов реакции и теми предположениями, которые были положены в основу статистических расчетов. [27]
 |
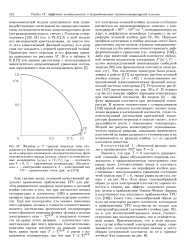
Динамика истощения ( / модели пласта длиной 5 м компонентами С5 и последующего вытеснения ( / / компонентов сухим газом. коэффициенты извлечения г г даны в % от. [28] |
На рис. 3.73 представлены результаты двух соответствующих экспериментов по вытеснению равновесной газовой фазы модели пласта сухим газом ( метаном) при температурах 20 и 62 С. Сравнение рис. 3.73 с рис. 3.71, 3.72 свидетельствует о существенном различии значений всех параметров продукции в случаях вытеснения пластовой смеси сухим газом из пласта, содержащего 12 5 и 2 % объема пор ЖУФ. [29]
Гастингс и Нихолсон [577] сравнили вычисленный и экспериментально найденный состав равновесной газовой фазы процесса изомеризации три - и тетраметилбензолов при 300 и 700 К и пришли к выводу, что данные совпадают в пределах, обусловленных возможными ошибками в анализе продуктов реакции и теми предположениями, которые были положены в основу статистических расчетов. [30]
Страницы: 1 2 3 4