Изучение - термодинамика
Cтраница 3
Эти сведения способствуют углублению изучения термодинамики и без знания их трудно понять некоторые принципиальные се особенности. Они являются также весьма полезными для лиц. [31]
Напротив, из результатов изучения термодинамики суперпарамагнитных частиц методом Монте-Карло [168] следует, что из-за отсутствия в этих частицах явно выраженного магнитного перехода нельзя говорить о каком-либо смещении температуры Кюри в зависимости от размера частиц. Действительно, переход наночастиц из суперпарамагнитного в парамагнитное состояние происходит плавно, без явно видимой резкой точки магнитного превращения. Измерения температуры Кюри наночастиц Ni ( d 1 5 нм) [171] и Со ( d 0, 8 нм) [172] показали, что эти величины в пределах погрешности измерений совпадают с таковыми для массивных металлов. Согласно [4,5] температура Кюри ферромагнитных частиц при уменьшении их размера до 2 нм не отличается от TC массивных металлов. Однако в [173] обнаружено понижение TC на 7 и 12 % для наночастиц Ni диаметром 6 0 и 4 8 нм соответственно. Следует отметить, что явление суперпарамагнетизма существенно затрудняет исследование зависимостей коэрцитивной силы, намагниченности насыщения и температуры Кюри ферромагнитных наночастиц от размеров. [32]
Это означает, что объектами изучения термодинамики становятся не только состояния равновесия или близкие к ним ( как это было в термостатике и термодинамике необратимых процессов), но и сравнительно далекие от них. [33]
В книге рассмотрены хроматографические методы изучения термодинамики растворов, а также другие неаналитические применения газовой хроматографии. В частности, освещены вопросы, имеющие большое теоретическое и практическое значение: определение коэффициентов активности при бесконечном разбавлении, определение вириальных коэффициентов в уравнении газового состояния и коэффициентов диффузии, изучение сорбционных свойств адсорбентов и катализаторов. [34]
Большая работа была выполнена по изучению термодинамики и кинетики оксо-реакции. Основные положения этого исследования сводятся к следующему. [35]
Для анализа кривых ДТА при изучении термодинамики неравновесных фазе переходов не может быть использована классическая линейная задача Д1 Л, основанна: решении уравнения теплопроводности Вместо треугольного импульса, вид кою определяется кинетикой подвода тепла к веществу постепенно от стенки сосуда к не образца, при контроле диссипативных процессов наблюдаются скачкообразные флуктуируи тепловые импульсы. Аналогичные результаты получены при исследовании на упан цифровою ДТА диссипативных процессов различной природы термогеиез пшеи мпцеллообразование в точке Крафта амфифилышх молекул, преципитация в кремни. [36]
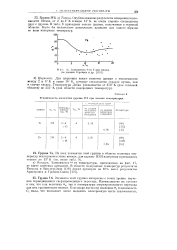 |
Теплоемкость элементов группы IV6 при низких температурах. [37] |
Элементы этой группы интересны с точки зрения изучения термодинамики сверхпроводящего перехода. Преимущество их состоит в том, что как величина Н, так и температуры сверхпроводящего перехода для них сравнительно велики. [38]
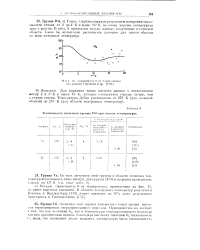 |
Теплоемкость элементов группы IV6 при низких температурах. [39] |
Элементы этой группы интересны с точки зрения изучения термодинамики сверхпроводящего перехода. Преимущество их состоит и том, что как величина W () 1 так и температуры сверхпроводящего перехода для них сравнительно велики. [40]
Понятие о больших молекулах возникло 3 при изучении термодинамики и гидродинамики коллоидных растворов новых классов химических соединений. [41]
В некоторых случаях ( например, при изучении термодинамики сорбции или при определении удельной поверхности твердых тел - катализаторов или адсорбентов) достаточно получить хроматографическую зону лишь одного вещества. [42]
Изобарный потенциал с большим успехом используется при изучении термодинамики химических реакций, так как его изменение выражает полезную работу при соблюдении легко выполнимых условий Tconsi и р - const. Эти условия являются весьма распространенными в химической практике. [43]
Изобарный потенциал с большим успехом используется при изучении термодинамики химических реакций, так как его изменение выражает полезную работу при соблюдении легко выполнимых условий Tconsi и р const. Эти условия являются весьма распространенными в химической практике. [44]
Из физико-химических применений газовой хроматографии следует отметить возможность изучения термодинамики сорбции, молекулярных весов, давления пара веществ, коэффициентов диффузии, поверхности адсорбентов и катализаторов. Широко применяются хроматографические методы определения элементного состава, а также методы определения констант химических реакций. [45]
Страницы: 1 2 3 4