Возрастание - атомный вес
Cтраница 2
Там с возрастанием атомного веса Mg, Zn, Cd, Hg легкоплавкость увеличивается, самый тяжелый металл - ртуть - даже представляет собой жидкость. Чтобы понять это, достаточно - пишет он - обратить внимание на элементы дальнейших групп нечетных рядов, напр. V группу, где Р, As, Sb, или на VI, где S, Se, Те, а также иа VII, где знакомые нам С1, Br, J. У них всех с возрастанием атомного веса легкоплавкость убывает; для них члены высшего ряда, или простые тела большого атомного веса, плавятся труднее, чем более легкие. [16]
Следовательно, с возрастанием атомного веса свойства элементов изменяются но непрерывно, а через определенное число элементов в основном повторяются, примерно так, как повторяются времена года. Такое изменение свойств носит название п е р и о д и ч с с кого. Периодическое изменение свойств элементов выступает очень наглядно, если оба рассмотренных ряда элементов расположить дру. [17]
 |
Кристаллические структуры кремния и алмаза. [18] |
Расположим элементы в порядке возрастания атомного веса и сравним их, что мы часто будем делать в этой главе. Вы едва ли сможете представить себе более разнообразные по внешнему виду вещества. Мы видим такие металлы, как натрий, магний и алюминий. Свежий срез образцов этих элементов имеет типичный металлический блеск. Металлы эти мягки, особенно натрий - его обычно режут ножом. Магний и алюминий можно сгибать руками, твердые предметы оставляют на них след. Кремний тоже имеет металлический блеск, но он гораздо тверже магния и алюминия. Одна из модификаций фосфора, называемая белым фосфором - бледно-желтое, похожее на воск твердое вещество с ярко выраженными неметаллическими свойствами. Черный фосфор, в который превращаются все другие формы фосфора под большим давлением, представляет собой темно-серое твердое вещество с металлическим блеском. Завершают период два газа - хлор и аргон, которые по внешнему виду, безусловно, совсем не похожи на металлы. [19]
Первый построен в порядке возрастания атомного веса элементов, второй - в порядке группирования элементов по их химическому сходству. [20]
Химическая активность галогенов с возрастанием атомного веса падает. Так, фтор соединяется с водородом со взрывом в темноте и без нагревания, хлор только на свету или при нагревании. Бром взаимодействует с водородом только при нагревании с получением прочного бромистого водорода, йод - только; при нагревании с получением непрочного йодистого водорода. [21]
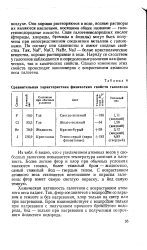 |
Сравнительная характеристика физических свойств галогенов. [22] |
Химическая активность галогенов с возрастанием атомного веса падает. Так, фтор соединяется с водородом со взрывом в темноте и без нагревания, хлор только на свету или при нагревании. Бром взаимодействует с водородом только при нагревании с получением прочного брошстого водорода, йод - только при нагревании с получением непрочного йодистого водорода. [23]
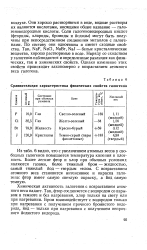 |
Сравнительн. ая характеристика физических свойств галогенов. [24] |
Химическая активность галогенов с возрастанием атомного веса падает. Так, фтор соединяется с водородом со взрывом в темноте и без нагревания, хлор только на свету или при нагревании. Бром взаимодействует с водородом только при нагревании с получением прочного бромистого водорода, йод - только при нагревании с получением непрочного йодистого водорода. [25]
Химическая активность галогенов ослабляется с возрастанием атомного веса. [26]
Атомная преломляемость этих элементов возрастает с возрастанием атомного веса. [27]
В 5 - 7 группах с возрастанием атомного веса элементов реакционная способность аналогичных ЭОС уменьшается. [28]
Эта группа, подобно предыдущей, с возрастанием атомного веса увеличивает энергию по отношению IK галоидам и уменьшает по отношению к О. Для всех этих металлов - щелочных и щелочноземельных - числа получены очень большие, далее следуют металлы тяжелые с числами гораздо меньшими. [29]
Исследуя химические элементы, Менделеев нашел, что постепенное количественное возрастание атомного веса необходимо вызывает коренное изменение химических свойств элемента: из одного качественного состояния совершается переход к другому качественному состоянию и, наоборот, качественное изменение с такой же необходимостью ведет к изменению количественных отношений элемента. [30]
Страницы: 1 2 3 4