Изучение - физическая адсорбция
Cтраница 1
Изучение физической адсорбции является очень важным средством исследования свойств гетерогенных катализаторов. Действительно, появление и начало широкого применения теории БЭТ ( разд. В настоящее время большинство наиболее употребительных методов определения величин поверхности все еще составляют методы, основанные на измерении физической адсорбции газа при температуре, близкой к температуре его кипения, хотя в них внесены некоторые усовершенствования, которые будут обсуждены ниже. Представления о физической адсорбции лежат в основе большинства многочисленных методов измерения пористости твердых тел; этот вопрос будет рассмотрен более детально позднее ( разд. Менее широко признается тот факт, что на основании изучения физической адсорбции можно делать заключения о том, какая часть поверхности твердого тела энергетически неоднородна. [1]
При изучении физической адсорбции обычно измеряют две характеристики: количество адсорбированного вещества и теплоту процесса. Изменение первой лежит в основе широко используемого метода БЭТ [2] и его модификаций при определении поверхности. Количество адсорбированного вещества на единицу веса адсорбента является функцией давления пара и температуры при постоянном объеме. Если объем системы изменяется с давлением, это необходимо принять во внимание. Зависимость количества адсорбированного вещества от давления при постоянных температуре и объеме называется изотермой адсорбции. [2]
При изучении полислойной физической адсорбции с целью измерения площади поверхности используют азот, гелий, криптон, бутан и другие газы. При этом определяют часть поверхности, которая доступна для соответствующих молекул. [3]
При изучении физической адсорбции бинарных смесей газов и паров на твердых адсорбентах удается обнаружить некоторые особенности адсорбционного поведения таких многокомпонентных систем, связанные со структурными характеристиками адсорбента. Исследование адсорбции смесей паров позволяет в ряде случаев получить более определенные выводы о механизме процесса сорбции и его связи со структурой адсорбента, чем это можно сделать на основании изучения изотерм адсорбции индивидуальных веществ. [4]
Одной из важнейших задач в области изучения физической адсорбции полимеров является установление связи между термодинамическими величинами, характеризующими процесс адсорбции, и экспериментальными, получаемыми при изучении различных систем. В случае высокомолекулярных систем данная задача намного усложняется по сравнению с низкомолекулярными системами из-за сложности термодинамического описания поведения гибких полимерных цепей в растворах и многочисленных, установленных экспериментально, особенностей адсорбции полимеров, которые определяются гибкостью полимерных цепей. [5]
Выражение (6.88) особенно важно для приложений в связи с изучением физической адсорбции и дифракции атомов на поверхности кристалла. Покажем здесь, следуя работе [21], что ван-дер-ваальсово взаимодействие атома ( или малой частички конденсированной фазы) с поверхностью возникает, по существу, по тем же причинам, которые приводят к взаимодействию между двумя атомами. В случае, которому отвечает формула (6.88), запаздыванием можно пренебречь. Тогда дело сводится к появлению пространственных корреляций между спонтанно флуктуирующими и индуцированными частями дипольного момента атома и поляризации в среде. [6]
В то время как газо-жидкостная хроматография позволяет изучать проблемы термодинамики растворов, газоадсорбционная хроматография позволяет перейти к изучению физической адсорбции. [7]
Отчасти по этой причине и отчасти потому, что недавно были опубликованы общие обзоры по данному вопросу, мы ограничимся здесь обсуждением результатов изучения физической адсорбции при известных степенях заполнений. С целью уменьшения рассеяния света гель был заключен в парафин. Не говоря уже о том, что парафин имеет в некоторых областях спектра полосы поглощения, недоступные для исследования, положение, вероятно, осложнялось тем, что он взаимодействовал с поверхностью геля. [8]
Значительно меньше исследований связано с характеристикой процесса физической адсорбции на основании данных исследования магнитной восприимчивости. Очевидно, при изучении физической адсорбции в качестве адсорбента должно быть выбрано пористое или высокодисперсное вещество, которое не способно в данных условиях вступать в химическое взаимодействие с молекулами адсорбата. [9]
Результаты измерения хемосорбции на поверхности катализатора могут в принципе дать количественную характеристику адсорбционной способности поверхности. Очевидно, что изучение хемосорбции позволяет сделать шаг вперед по сравнению с изучением физической адсорбции, так как получают информацию, скорее, об активной, а не об общей поверхности. Однако в некоторых случаях активная и общая поверхности оказываются тождественными. При изучении хемосорбции и ее роли в гетерогенном катализе обычно возможны два противоположных подхода. Согласно первому из них, выбирают такие условия эксперимента, при которых, как заведомо известно, катализ протекает эффективно, и изучают адсорбцию соответствующих газов на поверхности. [10]
В, БЭТ, Гаркинса и Юра, хорошо согласуются друг с другом, а также с результатами других, независимых измерений. Недостаток места не позволяет привести все данные, подтверждающие действенность этих методов, основанных на изучении физической адсорбции газов. [11]
В правильно сконструированной ячейке ( типичные размеры L13 CM, d 14 см) время прохождения молекулы азота составляет всего лишь около 1 мсек. Для выделения хемосорбированного газа, которое продолжается по крайней мере 150 мсек и для которого т мало, таким запаздыванием можно пренебречь. При десорбции низкотемпературной формы, завершающейся за 20 - 40 мсек, или для окиси углерода, у которой время жизни при адсорбции на стеклянных стенках представляет заметную величину, манометр может не дать мгновенного изображения процессов, происходящих вблизи образца. Эта трудность особенно сильно проявляется при изучении физической адсорбции. Например, при десорбции ксенон адсорбируется на проводах и стеклянных частях, которые также охлаждаются при охлаждении образца до температуры ( Г115 К), при которой протекает адсорбция. Чтобы компенсировать это, десорбция должна проводиться очень быстро, за время не больше - 10 мсек. Поскольку время запаздывания составляет около 1 мсек, даже без учета адсорбции, трудно количественно изучить кинетику десорбции. [12]
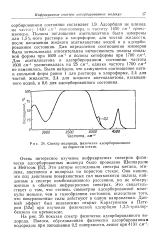 |
Спектр водорода, физически адсорбированного на пористом стекле. [13] |
Они нашли, что под действием поверхностных сил выявляются полосы, найденные в спектре комбинационного рассеяния, но не обнаруженные в обычных инфракрасных спектрах. Это свидетельствует о том, что степень симметрии адсорбированной молекулы меньше, чем в газообразном состоянии, вследствие того, что поверхностные силы действуют в одном направлении. Данный эффект был независимо открыт Карагунисом и Петером [ 52а ] при изучении физической адсорбции 1 3 5-трихлор-бензола на кремнеземе. [14]
Более сложные системы, в которых, например, молекулы адсорбата многоатомные, а решетка твердого тела уже не кубическая, требуют более трудоемких расчетов. Возможно, они будут связаны с необходимостью введения параметров, значения которых можно определить. Кроме того, необходимо иметь в виду, что результаты всех подобных расчетов ( включая рассматриваемую адсорбцию аргона на хлориде калия) сильно зависят [20] от выбора значения г0 - равновесного расстояния адсорбированного атома или молекулы от поверхности. Это расстояние трудно определить непосредственно из-за неопределенности в вопросе о том, как расположена по отношению к центрам ионов поверхностного слоя плоскость, представляющая поверхность твердого тела. Однако для систем, встречающихся при изучении физической адсорбции, зависимость потенциальной энергии от расстояния в целом имеет тот же самый вид, что и в случае адсорбции аргона на хлориде калия, представленном на рис. 7, и поэтому применимы все рассуждения, касающиеся природы адсорбционного слоя. [15]
Страницы: 1 2