Калориметрическое изучение
Cтраница 1
Калориметрическое изучение производилось в калориметре, описанном выше, в камере моей конструкции, устройство которой также было описано. [1]
Калориметрическое изучение возможности получения регулярно чередующегося бутадиенпропиленового сополимера путем полимеризации 4-метилциклогексена с раскрытием цикла. [2]
Калориметрическое изучение растворения безводной соли аналогично изучению растворения кристаллогидрата. Учитывая гигроскопичность безводной соли, максимально ограничивают время контакта соли с атмосферой. [3]
Калориметрическое изучение фазовых переходов асфальтено-ароматических смесей, наполненных трикозаном / / Журн. [4]
Калориметрическое изучение кинетики термического разложения твердых веществ свободно от ряда принципиальных недостатков, присущих таким классическим методикам, как термогравиметрия или волюметрия. Так, например, наличие диффузионных затруднений при выходе газообразных продуктов реакции из конденсированной среды в двух последних методиках приводит к получению заниженного значения константы скорости, в то время как в калориметрическом опыте, в случае существенно необратимой реакции, фиксируется мощность, соответствующая истинной кинетике. [5]
Энергию обмена при калориметрическом изучении процесса измеряют главным образом в виде теплоты. В некоторых экспериментах требуется измерять и другие виды энергии, например, в деформационной калориметрии - энергию перемещения ( механическую работу), в других случаях - поверхностную энергию и энергию сжатия. [6]
Для определения теплоты образования гидрата фосфата празеодима был использован калориметр с изотермической оболочкой [ 2j Калориметрическое изучение теплоты растворения этой соли затруднено вследствие ее плохой растворимости в воде и растворах кислот. [7]
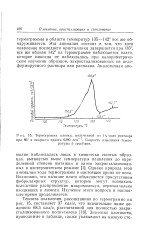 |
Термограмма пленки, полученной из 1 % - ного раствора при 86 и скорости сдвига 6290 сек - Скорость изменения температуры 5 град / мин. [8] |
Эта аномалия состоит в том, что хотя плавление последнего кристаллика завершается при 135, все же вблизи 142 на термограмме наблюдается плато, которое никогда не наблюдалось при калориметрическом изучении образцов, закристаллизованных из неде-формируемого раствора или расплава. [9]
К другому выводу относительно расположения атомов в гидриде палладия приходят Найс и Астон в своих работах [517 - 519], выполненных методом изучения равновесной упругости водорода и теплоты образования сплавов по данным непосредственного калориметрического изучения. При повышении температуры наблюдаются равновесия. [10]
В связи с разработкой промышленной технологии синтеза лактида, его полимеризации и переработки образующегося полимера необходимо изучение термодинамических свойств лактида, полилактида и термодинамических критериев процессов получения и полимеризации лактида в широкой области температур. В данной работе впервые выполнено калориметрическое изучение термодинамических свойств / - лактида в области 0 - - 430 К при нормальном давлении. По полученным данным рассчитаны функции Н ( Т) - Я ( 0), S ( Т), Jf ( T) - Я ( 0) для указаннной области температуры; АЯ /, А5 /, ДО0 / для стандартных Т и р; энтальпия ( АН0), энтропия ( AS) и энергия Гиббса i ( A 0) процесса получения - лактида путем дегидратации / - молочной кислоты. [11]
 |
Зависимость эффективной теплоты радиационной полимеризации QJ ММА ( а и АН ( б на силикагеле КСК от концентрации адсорбированного мономера 0 при 20 С и мощности дозы 0 1 ( а и 0 3 Гр / с ( б. [12] |
Экспериментально вопрос о термодинамических особенностях полимеризации на поверхности изучен явно недостаточно. Согласно проведенному в работах [161, 162] калориметрическому изучению полимеризации ряда мономеров ( АН, ММА, тетрафторэтилен), адсорбированных на силикагеле КСК-2, эффективные теплоты полимеризации б в области небольших заполнений поверхности мономером очень значительно отличаются от значений б при полимеризации тех же мономеров в жидкой фазе. [13]
Теплоты атомизации данных соединений были найдены при калориметрическом изучении реакций с участием хлортрифторэтилена. Систематические расхождения между экспериментальными и расчетными данными превосходят возможные ошибки опыта, и это наводит на мысль, что теплота образования хлортрифторэтилена может оказаться очень высокой. [14]
Слагаемые, стоящие в (5.30), (5.31) под знаком суммы, учитывают влияние изменений химического состава на теплоемкость и скрытую теплоту расширения. Значения Су и Cv, n в ряде случаев могут быть получены экспериментально. Например, калориметрическое изучение смеси газообразного водорода и кислорода при низких температурах в отсутствие катализатора позволяет определить CV n этой смеси; если же в систему ввести катализатор, она станет равновесной и аналогичный, эксперимент даст уже значение Су. [15]
Страницы: 1 2