Электрохимическая адсорбция
Cтраница 1
Электрохимическая адсорбция, как показал Д. Н. Стражеско [1015], может быть применена, как метод выделения, очистки и концентрирования микроколичеств растворенных ионов. Например, катионы адсорбируют на угле в атмосфере водорода, переносят этот уголь в малый объем воды и де-сорбируютвнее эти же катионы, меняя водородную атмосферу на кислородную. [1]
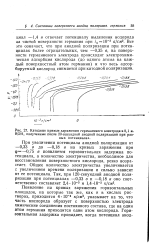 |
Катодные кривые заряжения германиевого электрода в 0 1 н. КОН, полученные после 20-секундной анодной поляризации при разных потенциалах. [2] |
Все это означает, что при анодной поляризации при потенциалах более отрицательных, чем - 0 35 в, на поверхности германиевого электрода происходит электрохимическая адсорбция кислорода ( до одного атома на каждый поверхностный атом германия) и что весь адсорбируемый кислород снимается при катодной поляризации. [3]
По аналогичным соображениям можно ожидать предельного тока при адсорбционно-электрохимическом механизме при безбарьерной электрохимической десорбции: в этом случае скоростью ионизации адсорбированных атомов ( реакция, обратная разряду ионов хлора) можно при не слишком катодных потенциалах пренебречь, а реакция электрохимической адсорбции должна быть безактивационной. [4]
Процессы сольватации и переноса протона в растворах посвящена подробному рассмотрению проблемы идентификации протона в растворе и кинетики электрохимической реакции его гомогенного переноса. Специальное внимание уделено рассмотрению электрохимической адсорбции, что делает изложение вопроса более полным и дает возможность западному читателю ознакомиться с уровнем и оригинальностью работ русских исследователей в этой области. Главу, посвященную механизму осаждения металлов, выгодно отличает от более ранних работ высокий уровень кинетического анализа. Наконец, в главе об адсорбции промежуточных частиц в электрокатализе дан обзор применяемых в настоящее время методов исследования адсорбции промежуточных радикалов в последовательных электродных реакциях и дается количественная кинетическая трактовка вопроса, которая может служить основой для интерпретации поведения более сложных промежуточных частиц, участвующих в реакциях окисления органических веществ. [5]
Если использовать экспериментальные данные о степени заполнения поверхности адсорбированными атомами водорода, то можно сделать достаточно вероятные предположения о том, каким путем преимущественно совершается отвод адсорбированных водородных атомов. Скорость разряда на адатомах водорода ( электрохимическая адсорбция) зависит от поверхностной концентрации водородных атомов в первой степени, а скорость рекомбинации - во второй. Поэтому на металлах, слабо адсорбирующих водород, удаление его с поверхности должно осуществляться главным образом за счет электрохимической десорбции. [6]
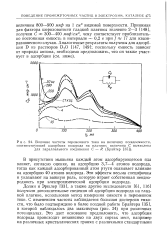 |
Влияние частоты переменного тока на величину псевдоемкости. [7] |
В присутствии мышьяка каждый атом адсорбирующегося яда влияет, согласно оценке, на адсорбцию 3 7 - 4 атомов водорода, тогда как каждый адсорбированный атом ртути оказывает влияние на адсорбцию 40 атомов водорода. Эти эффекты весьма специфичны и указывают на важную роль, которую играет собственная неоднородность при электрохимической адсорбции водорода. [8]
Рассмотрим механизм разряд-электрохимическая десорбция. Если медленным является безбарьерный разряд, то не может наблюдаться предельный недиффузионный ток катодного восстановления порядка тока обмена: скорость обычной электрохимической адсорбции с ростом потенциала будет непрерывно возрастать, а скорость ионизации образующихся при этом адсорбированных атомов будет расти, несмотря на безактивационный характер реакции ионизации, благодаря непрерывному росту их концентрации. Иными словами, если в анодной области мы наблюдали медленный безбарьерный разряд, а скорость электрохимической десорбции автоматически устанавливалась такой, чтобы обеспечить стационарность концентрации адсорбированного хлора, то катоднее равновесного потенциала роль определяющей скорость стадии переходит к электрохимической адсорбции, а скорость ионизации теперь, в силу стационарности процесса, подстраивается к этой стадии. [9]
Он писал: При работе с водными растворами выбор адсорбента крайне ограничен, так как адсорбент должен быть практически нерастворим в среде адсорбции. При адсорбции из водных растворов должно проявляться зачастую то, что Михаэлис и Эренрейх называют электрохимической адсорбцией и что, в сущности, не что иное, как химическое соединение ( 1910в, стр. [10]
Рассмотрим механизм разряд-электрохимическая десорбция. Если медленным является безбарьерный разряд, то не может наблюдаться предельный недиффузионный ток катодного восстановления порядка тока обмена: скорость обычной электрохимической адсорбции с ростом потенциала будет непрерывно возрастать, а скорость ионизации образующихся при этом адсорбированных атомов будет расти, несмотря на безактивационный характер реакции ионизации, благодаря непрерывному росту их концентрации. Иными словами, если в анодной области мы наблюдали медленный безбарьерный разряд, а скорость электрохимической десорбции автоматически устанавливалась такой, чтобы обеспечить стационарность концентрации адсорбированного хлора, то катоднее равновесного потенциала роль определяющей скорость стадии переходит к электрохимической адсорбции, а скорость ионизации теперь, в силу стационарности процесса, подстраивается к этой стадии. [11]
Толщина такого слоя, составляющая по данным [162] 0 05 мкм ( сплошной слой никеля), достаточна для закрепления частиц А12О3 размерами до 150 мкм. Эти величины, видимо, пропорциональные степени дисперсности частиц, характерны для физической адсорбции, из чего можно допустить, что перехода от слабой физической адсорбции частиц к поверхности к более сильной, очевидно, не существует, поскольку при наращивании металла не наступает электрохимическая адсорбция, а происходит захват частиц постепенно изменяющимся по структуре электрокристаллизуемым слоем металла. Проведение опытов с поляризацией в отсутствие разряда металла [162] ( раствор Na2SO4) или с разрядом меди [121, 155] или кадмия [120] показало, что при наличии тока число адгезированных на поверхности частиц может уменьшиться. [13]
Катодный процесс разряда и выделения водорода был детально исследован, особенно школой акад. Общая реакция катодного разряда водорода 2H - t - 2e - - H2 представляет собой ряд последовательно связанных стадий. Установлено, что в большинстве случаев стадией, наиболее тормозящей общий процесс, для многих металлов является передача заряда. Только для некоторых металлов с низким перенапряжением водорода - платины и палладия - основной тормозящей стадией может быть рекомбинация атомов водорода или их электрохимическая адсорбция. Остальные ступени, как, например, концентрационная поляризация ( затруднение в подводе ионов водорода к электроду и отвод атомов или молекул водорода) вследствие большой подвижности ионов водорода и возможности его выделения в виде пузырьков газа, оказывают незначительное торможение, особенно, если процесс происходит в кислой среде. [14]
Страницы: 1