Термодинамическое изучение
Cтраница 1
Термодинамическое изучение протекающих в каолинах процессов показало наличие при температуре до 1000 С двух тепловых эффектов: при 550 - 800 С - эндотермического, которому соответствует дегидратация, и около 980 С - экзотермического. [1]
Термодинамическое изучение реакций, протекающих, например, в каолинах в производстве фарфора, показало наличие при нагреве до 1000 С двух тепловых эффектов: при 550 - 800 С - эндотермического и при 980 С - экзотермического, что важно знать для правильного расположения теплогенераторов и тешюотводящих устройств в печи. [2]
Термодинамическое изучение реакции (1.1) [5] и сходного случая образования гидрида переходного металла, представленного реакцией (1.2) [8], показывает, что энергия связи металл - водород примерно равна 250 кДж / моль. [3]
Термодинамическое изучение равновесия между жидкостью и паром значительно облегчается, если к паровой фазе возможно применить законы идеальных газов. Физически идеальный газ можно определить как совокупность частиц, взаимодействие между которыми пренебрежимо мало. Модель идеального газа с хорошей степенью точности описывает свойства реальных разреженных газов, в которых средние расстояния между частицами много больше диаметра молекулы. [4]
Термодинамическое изучение взаимодействия растворенное вещество-растворитель с использованием газо-кидкостной хроматографии. [5]
Термодинамическое изучение комплексов меди с М - ( 2-аминоэтил) - мор-фолином. [6]
Термодинамическое изучение ионной полимеризации стирола5122 5123 позволило установить5122, что при различных равновесных концентрациях мономера в хорошем и плохом растворителе величины свободной энергии одинаковы. И для перехода жидкий мономар-кгвердый полимер найдено: ЛЯ - 17 400 ккал, a AS - 24 8 энтр. [7]
Термодинамическое изучение растворов электролитов в органических жидкостях пока ведется недостаточно. Политермические измерения осуществляются только в нашей лаборатории. При 25 С интересные результаты по термодинамике неводных и водно-неводных солевых растворов получены Г. А. Крестовым с сотрудниками, О. Я. Самойловым с сотрудниками, С. И. Дракиными др. За рубежом такого рода работы немногочисленны. [8]
Термодинамическое изучение растворов электролитов в органических жидкостях пока ведется недостаточно. Политермические измерения осуществляются только в нашей лаборатории. При 25 С интересные результаты по термодинамике неводных и водно-неводных солевых растворов получены Г. А. Крестовым с сотрудниками, О. Я. Самойловым с сотрудниками, С. И. Дракиным и др. За рубежом такого рода работы немногочисленны. После выполненных еще в 30 - х и 40 - х годах измерений Вольфендена с сотрудниками и Слан-ского в последние годы мы находим в литературе только отдельные работы по теплотам растворения в органических средах, проведенные при 25 С и в ограниченной зоне разбавленных растворов ( С. [9]
Термодинамическое изучение растворов электролитов в органических жидкостях пока ведется недостаточно. Политермические измерения осуществляются только в нашей лаборатории. При 25 С интересные результаты по термодинамике неводных и водно-неводных солевых растворов получены Г. А. Крестовым с сотрудниками, О. Я. Самойловым с сотрудниками, С. И. Дракиными др. За рубежом такого рода работы немногочисленны. [10]
Из термодинамического изучения растворов электролитов мы обычно получаем значения средних коэффициентов активности у для комбинации ионов. [11]
Из термодинамического изучения растворов электролитов мы обычно получаем значения средних коэффициентов активности Y для комбинации ионов. [12]
При термодинамическом изучении пленок можно применять методы и приемы, разработанные для поверхностей разрыва. В горных породах мы рассматриваем адсорбционные пленки, относящиеся к классу неавтономных пленок, поскольку при отделении от адсорбента они становятся неустойчивыми. В связи с тем, что состав и структура адсорбционных пленок обусловливаются полем адсорбента электрической природы, их состояние не может быть охарактеризовано без учета внешнего поля. Другая особенность адсорбционных пленок заключается в том, что обмен происходит между составляющими их компонентами и одной из контактирующих фаз. [13]
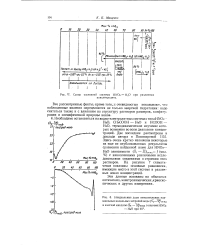 |
Неидеальные доли относительных парциальных модальных энтропии воды ( Sx - Sj / неид и азотной кислоты ( 82 - З неид в системе HNO3 при 40. [14] |
НЮ, термодинамическое изучение которых возможно во всем диапазоне концентраций. [15]
Страницы: 1 2 3 4