Кинетическое изучение - реакция
Cтраница 1
Кинетическое изучение реакций на примере полифторарома-тических соединений позволило установить, что взаимодействие их с алкоголятами металлов в жидком аммиаке протекает с существенно большей скоростью, чем в спиртах. [1]
Кинетическое изучение реакции сильно осложняется, если точность определения зависимости между скоростью и глубиной протекания реакции невелика. В таком случае описание процесса целиком основывается на зависимости между глубиной протекания реакции и временем. [2]
Кинетическое изучение реакции Фриделя-Крафтса провести нелегко, поскольку скорость очень чувствительна к следам влаги, реакционная смесь расслаивается в негомогенные слои, первоначальные продукты реакции легко изомеризуются, и, кроме того, кинетика сильно зависит от растворителя. Несмотря на эти трудности, основные закономерности этой реакции в настоящее время достаточно хорошо выяснены. Например, беизилирование хлористым бензилом в нитробензоле в присутствии безводного А1С1з в качестве катализатора описывается кинетическим уравнением третьего порядка. [3]
Кинетическое изучение реакции Фриделя-Крафтса провести нелегко, поскольку скорость очень чувствительна к следам влаги, реакционная смесь расслаивается в негомогенные слои, первоначальные продукты реакции легко изомеризуются, и, кроме того, кинетика сильно зависит от растворителя. Несмотря на эти трудности, основные закономерности этой реакции в настоящее время достаточно хорошо выяснены. Например, бензилирование хлористым бензилом в нитробензоле в присутствии безводного А1С13 в качестве катализатора описывается кинетическим уравнением третьего порядка. [4]
 |
Реакция триэтиламина с тетрахлор-п-бензохиноном. [5] |
Кинетическое изучение реакции дигидропиридинов с 2 6-дихлорфенолиндофенолом и другими хинонами в буферном растворе в 50 % - ном метаноле, проведенное Уолленфелсом и Гелрихом [187], также не позволило сделать выбор между двумя возможными механизмами, однако было установлено, что многие из этих реакций протекают с измеримой скоростью. По-видимому, в этой реакции должен происходить одноэлектронный переход. [6]
Кинетическое изучение реакции гидролиза на примере ме-тил-бис - ( р-хлорэтил) амина в водном спирте показывает [60, 68, 71, 75], что в течение первого получаса идет образование 1-ме-тил - 1 - ( - хлорэтил) этилениминиевых ионов, которое сопровождается выделением С1 - - ионов и возрастанием тиосульфатного титра раствора. Скорость отщепления С1 - - ионов подчиняется уравнению реакции первого порядка с энергией активации - 18 ккал / моль. Затем происходит постепенное снижение тиосульфатного титра раствора в результате гидролитического размыкания этилениминных циклов. В присутствии щелочи отмеченная кинетическая картина существенно изменяется. [7]
Первое детальное кинетическое изучение реакции аминолиза было проведено Беттсом и Гамметом [132], которые исследовали аминолиз толилацетатов в абсолютном метаноле. [8]
При кинетическом изучении реакции первого порядка вместо концентраций можно использовать любые другие величины, которые меняются пропорционально концентрации. [9]
Обязательной стадией кинетического изучения реакции является определение порядков реакции по реагентам. [10]
Последняя осуществлялась при проведении кинетического изучения реакции алкилирования - бутана пропиленом с целью построения адекватной кинетической модели этой реакции. [11]
 |
Кинетические кривые реакции дегидрохлорирования на начальных стадиях процесса распада ПВХ. [12] |
Вообще говоря, при количественном кинетическом изучении реакций твердых полимеров имеются ощутимые трудности. Для ПВХ они связаны кроме отмеченного выше, с тем, что полимер, хотя и размягчается при нагревании, однако при температуре деструкции его отдельные частицы не теряют своей формы и не могут свободно течь. Эти трудности усугубляются еще и тем, что после протекания реакции до сравнительно небольшой глубины остаток становится очень хрупким и неплавким. Если не принимать специальные меры для поддержания требуемой температуры во всей массе полимера, передача тепла в деструктиру-ющий материал может легко стать фактором, определяющим скорость процесса, что приведет к получению совершенно неправильных результатов. [13]
 |
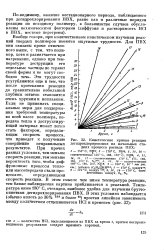
Сравнение скоростей адсорбции кислорода ( 1 и взаимодействия водорода в адсорбированным кис-л ородом ( 2 со скоростью реакции окисления в стехиометрическойсмеси Н. и О2 ( 3 при 135 С. [14] |
На рис. 3 приведены результаты кинетического изучения реакций ( 1), ( П) и ( III) на золоте при 120 С. Скорость адсорбции молекулярного кислорода па чистой поверхности золота при 120 С и давлении 0 1 мм рт. ст. составляет - 2 5 - 10п атомов 0 / сек-см Аи. Вплоть до адсорбции 0 05 сж3Оа / лгАи скорость адсорбции практически не изменяется, затем снижается довольно быстро и при покрытии выше 0 20 сл 02 / л2 Аи составляет - 2 - 109 атомов О / сек - см2 Аи. При адсорбции до 0 09 см802 / м2 Аи скорость адсорбции пропорциональна давлению кислорода в первой степени. [15]
Страницы: 1 2