Форма - адсорбционная изотерма
Cтраница 1
Форма адсорбционной изотермы тесно связана с механизмом самого процесса адсорбции. [1]
Вопрос о форме адсорбционной изотермы тесно связан с теорией адсорбции. Особенно важно изучение крайних участков кривой. Если адсорбция не ограничивается мономолекулярным слоем, то после полного покрытия им поверхности насыщение не достигается, а с увеличением давления адсорбция неограниченно растет за счет многослойного покрытия и капиллярной конденсации. Это большей частью и наблюдается при адсорбции паров и др. С другой стороны, в области малых давлений, когда заполнение поверхности очень мало, нельзя ожидать ни образования полимолекулярных слоев, ни значительного взаимодействия частиц на поверхности. Поэтому, независимо от правильности упомянутых допущений элементарной теории, начальный участок адсорбционной изотермы должен, в согласии с уравнением Лэнгмюра, быть прямолинейным, и нарушение этой линейности должно свидетельствовать о наличии дополнительных факторов, которые следует учитывать при разработке общей теории адсорбции. [2]
Вопрос о форме адсорбционной изотермы тесно связан с теорией адсорбции. Особенно важно изучение крайних участков кривой. [3]
Иначе говоря, мы предполагаем, что форма адсорбционной изотермы, определяемая видом функции f ( 9), не зависит от потенциала электрода. [4]
Для того чтобы можно было сделать вывод о форме адсорбционной изотермы, нужно, чтобы было выполнено условие обратимости процесса адсорбции. Критерием может служить совпадение хода прямой и обратной поляризации. Если это условие будет выполнено, что удается значительно лучше в случае адсорбции водорода, чем в случае кислорода, то мы действительно получаем адсорбционную изотерму, измеренную электрохимическим путем. Если условие обратимости строго не выполнено, то средняя кривая, проведенная между кривой прямой и обратной поляризации, может дать приближенное представление о форме адсорбционной изотермы. [5]
Предсказываемая уравнением ( 71) линейная зависимость емкости от количества адсорбированного вещества проверялась Парсон-сом в 1959 г. [70] в связи с формой адсорбционной изотермы. [6]
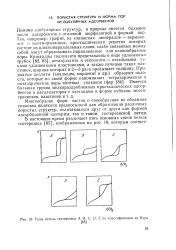 |
Типы петель гистерезиса А, В, С, D, Е по классификации де Bvpa. [7] |
Многообразие форм частиц и своеобразная их объемная упаковка являются предпосылкой для образования различных пористых структур, отличающихся друг от друга как формой адсорбционной изотермы, так и типом гистерезисной петли. [8]
При очень высоких заполнениях, когда молекулы адсорбата расположены близко друг от друга, существенную роль могут играть лондоновские дисперсионные силы. Однако при столь высоких значениях 6 форму адсорбционной изотермы определяет в основном предэкспо-ненциальный член [ ленгмюровский, ср. [9]
Так, сплошные и пунктирные линии на рис. 1 рассчитаны теоретически для двух различных фонов, а точками нанесены значения а, полученные из ширины пиков на С-ф-кривых ( после введения поправок на неравновесность и на зависимость а от рН раствора), а также по форме адсорбционной изотермы при потенциале максимальной адсорбции. Как было показано в [2], С - ф - и а-ф-кривые, рассчитанные по обобщенной модели поверхностного слоя и по модели двух параллельных конденсаторов е учетом произвольной зависимости а от ф, практически Совпадают. Поэтому для всех кислот расчет С - ф - и а-ф-кривых выполнялся более простым вторым методом, подробно описанным в гл. Хорошее согласие между расчетом и опытом наблюдалось во всех исследованных системах и иллюстрируется рис. 2 на примере н-валериановой кислоты. [10]
Использование уравнения ( 46а), не являющегося чисто термодинамическим, для изучения изотерм адсорбции вызвало возражение Парсонса [184], однако высказанные нами выше соображения относительно уравнения ( 9) дают основание использованию емкостных измерений для изучения изотерм адсорбции органических соединений на поверхности электрода. В работе Лайтинеиа и Мозьер [185] этим методом были изучены изотермы адсорбции на ртути тридцати различных органических веществ, причем было отмечено, что форма их приблизительно соответствует форме изотермы Ленгмюра. Это ограничивает значение выводов, относящихся к форме адсорбционной изотермы. [11]
В равновесных условиях при а 2 наблюдается скачкообразный переход от разреженного газообразного слоя с малой степенью заполнения к конденсированной пленке, для которой 9 близко к единице. Следует, однако, отметить, что уравнение ( 48), выведенное на основании чрезвычайно упрощенных допущений, может претендовать лишь на полу количественное истолкование явлений, происходящих в области двухмерной конденсации, которые, несомненно, имеют более сложный характер. Некоторые расхождения, возможно, связаны с тем, что нами не учитывалось изменение коэффициента активности с ростом концентрации органического вещества, вследствие чего несколько искажалась форма адсорбционной изотермы. [12]
Для того чтобы можно было сделать вывод о форме адсорбционной изотермы, нужно, чтобы было выполнено условие обратимости процесса адсорбции. Критерием может служить совпадение хода прямой и обратной поляризации. Если это условие будет выполнено, что удается значительно лучше в случае адсорбции водорода, чем в случае кислорода, то мы действительно получаем адсорбционную изотерму, измеренную электрохимическим путем. Если условие обратимости строго не выполнено, то средняя кривая, проведенная между кривой прямой и обратной поляризации, может дать приближенное представление о форме адсорбционной изотермы. [13]
Страницы: 1