Нестабильная форма
Cтраница 3
Что касается воздействия гидроксил-иона, то невозможно понять, как он мог катализировать растворение стишовита, в котором атом кремния уже достиг своего максимального координационного числа. Нет убедительных данных, показывающих влияние рН на скорость растворения стишовита, но интересно, что при рН 8 4 он растворяется примерно с той же скоростью, что и кварцевое стекло, если сравнивать равные по величине площадки на поверхностях, подвергавшихся действию раствора. Более того, стишовит продолжал растворяться после того, как был пройден уровень насыщения кварцевого стекла или аморфного кремнезема. Похоже, что стишовит представляет собой гидролитически нестабильную форму и в конечном счете должен полностью распадаться до аморфного кремнезема. Оказывает ли величина рН влияние на скорость гидролиза стишовита, остается неизвестным. [31]
Последействие не может быть вызвано медленным действием свободных радикалов, производимых излучением, потому что они живут недостаточно долго. Это наводит на мысль, что последействие, возможно, вызвано медленной реакцией поврежденной излучением нуклеиновой кислоты с перекисью водорода, дающей свободные гидроксильные радикалы, которые могут уменьшать вязкость неповрежденной нуклеиновой кислоты. Однако имеются три довода, показывающие, что это объяснение не может быть полным. Во-вторых, защитные вещества, как уже отмечалось, не могут ингибировать последействие, когда они добавлены после облучения. Очевидно, при облучении нуклеиновая кислота превращается в нестабильную форму. [32]
Гидроксиды металлов осаждаются обычно не в чистом виде, а в соединении с некоторой долей неразложившейся соли - в форме основной соли. Примером может служить осаждение из хлоридных или сульфатных растворов гидроксида магния, который выделяется в виде основных солей непостоянного состава. Особенно прочные основные соли образуются при осаждении из сульфатных растворов. Избыток щелочи разлагает основные соли, но не всегда в полной мере. Вследствие больших пересыщении при осаждении и очень быстрого ( мгновенного) образования твердой фазы, она часто выделяется вначале в нестабильной форме, неравновесной с раствором. При дальнейшем контакте составы осадка и раствора постепенно изменяются и приходят в равновесие. Этот процесс иногда называют старением осадка. [33]
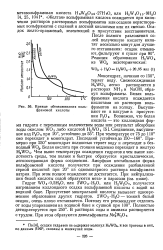 |
Кривые обезвоживания вольфрамовой кислоты. [34] |
Моногидрат, начиная со 150, теряет воду. Свежеосажденная H2WQ4 легко растворяется в растворах NH3 и NaOH, образуя вольфраматы. Белая вольфрамовая кислота осаждается кислотами из растворов вольфраматов на холоду. При температуре от 75 до 110 оно переходит в моногидрат. Чем выше температура осаждения гидратов и чем выше кислотность среды, тем полнее и быстрее образуется кристаллическая, легкооседающая форма соединения. Аморфная нестабильная форма вольфрамовой кислоты получается при осаждении разбавленной серной кислотой при 20 из одномолярного раствора вольфрамата натрия. При этом полное осаждение не достигается. [35]
Обычно техника такого эксперимента состоит в следующем. На исследуемое вещество, которое может находиться как в газообразной, так и в конденсированной фазе, действуют вспышкой света-возбуждающая вспышка ( энергия каждой вспышки достигает 5000 дж, а ее продолжительность-около 10 - 3 сек. Свет второй вспышки проходит через облучаемое вещество и анализируется спектральным методом. Любые нестабильные формы, образовавшиеся в результате первой вспышки, можно обнаружить по изменениям, которые они вносят в спектр поглощения исследуемого вещества. Время жизни нестабильных форм можно измерить, изменяя промежуток времени между возбуждающей и зондирующей вспышками. Основные экспериментальные трудности описанного метода заключаются в следующем. [36]
Появление продуктов распада в микроструктуре всегда служит предостережением против применения рентгеновского метода; однако отсутствие продуктов распада вовсе не означает, что его можно надежно применять. В некоторых системах, в которых определенная фаза стабильна только при высоких температурах, закалка может вызвать фазовое превращение. Новая фаза может оказаться нестабильной. Так, в сплаве меди с галлием с содержанием галлия примерно 27 % ( атомн. Таким образом, рассматриваемый сплав в условиях равновесия никогда не бывает только в виде гомогенной плотноупакованной гексагональной фазы, и образование при закалке однофазной структуры является следствием превращения в нестабильную форму. При этих условиях метод микроанализа все же позволяет правильно установить границы фаз, потому что если даже одна фаза полностью претерпевает при закалке превращение, то между сплавами, которые были соответственно гомогенными и двухфазными при температуре закал. Рентгеновское исследование закаленных образцов в таких случаях может привести к оши-б Ьчным выводам, и поэтому почти всегда лучше применять методы микроанализа и рентгеновский совместно, а не полагаться только на последний. В описанном выше случае может быть применено рентгеновское исследование в высокотемпературной камере. [37]
Страницы: 1 2 3