Ионная форма
Cтраница 3
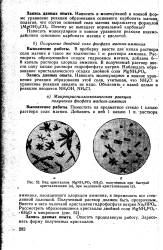 |
Вид кристаллов MgNH4PO4 6Н2О, полученных при быстрой кристаллизации ( а -, при медленной кристаллизации ( 6. [31] |
Написать в молекуляной и ионной форме уравнение реакции образования основиогр карбоната магния, полагая, что состав основной соли магния выражается формулой. Почему не выпадает нормальный карбонат. [32]
Напишите в молекулярной и ионной форме уравнения всех реакций, которые вы наблюдали, а также уравнение реакции перехода Ве ( ОН) 2 в новую труднорастворимую форму Ве2О ( ОН) 2, которая получается из Ве ( ОН) 2 при стоянии. [33]
Выписываем в ионной форме уравнения полуреакций восстановления окислителя и окисления восстановителя. [34]
Составьте в ионной форме уравнения реакций получения солей мета -, пиро - и ортованадиевых кислот. [35]
Различие между молекулярной и ионной формой записи реакций замещения состоит в том, что принимают существующими в шлаке и реагирующими с металлом или молекулы свободных окислов, или ионы. Стрелки в уравнениях реакций показывают, что взаимодействие может идти в обоих направлениях. [36]
Установлено, что ионная форма и скорость деформации мембран практически не влияют на их механические свойства. [37]
Для вычисления содержания ионных форм СО2 используются результаты определения общей ( т) и свободной ( р) щелочности. При алкалимегрическом титровании до рН 8 3 карбонат-ионы реагируют с кислым титрованным раствором с образованием гидрокарбонатов. [38]
 |
Граничные поверхности. [39] |
К - вклад ионной формы, оказывается ниже по энергии, чем VKOB и У т в отдельности. Такое явление называется ковалентно-ионным резонансом ( подробное обсуждение дано в разд. [40]
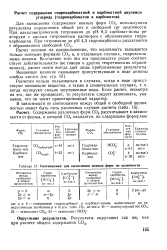 |
Соотношения для вычисления ионных форм по щелочности. [41] |
Для вычисления содержания ионных форм СО2 используются результаты определения общей ( т) и свободной ( р) щелочности. При алкалиметрическом титровании до рН 8 3 карбонат-ионы реагируют с кислым титрованным раствором с образованием гидрокарбонатов. [42]
Если образующийся из ионной формы твердый силикат не заполняет поры, то подобная гелю сетка из частиц будет давать усадку и в пленке начнут развиваться трещины. [43]
При необходимости определения ионной формы обменника производят анализ элюата. [44]
Для изучения заряда ионных форм радиоэлемента наиболее простыми являются методы Стрикленда и Трофимова, так как они основаны на измерении радиоактивности равновесного с ионитом раствора. Метод Сэлмана, основанный на измерении радиоактивности твердой фазы ионита, является громоздким и неудобным для практического применения. Кроме того, не всегда состав соединений, поглощаемых ионитом, отвечает составу исходного раствора и это обстоятельство требует весьма осторожного отношения к результатам работ по методу Сэлмана. [45]
Страницы: 1 2 3 4