Закисная форма
Cтраница 1
Закисная форма может переходить в окисную вследствие контакта пластовой воды с кислородом воздуха или пресными водами или при изменении рН воды. Из 1 г трехвалентного железа при коагуляции образуется 1 83 г осадка гидроокиси железа, который занимает объем 5 мл. Для окисления 1 г трехвалентного железа достаточно 0 14 г кислорода. [1]
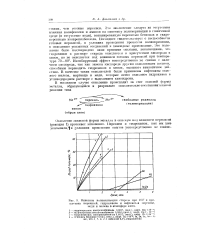 |
Кинетика полимеризации стирола при 100 в присутствии перекисей, гидрохинона и нафтенатив марганца, меди и железа в атмосфере азота. [2] |
Окисление закисной формы металла в окисиую иод влиянием перекисей ( реакция 1) протекает мгновенно. [3]
Наличие в трубопроводах закисных форм железа, которые образуются в результате разрушения материала труб, способствует развитию железобактерий, жизнедеятельность которых связана с процессом окисления железа. Кроме того, присутствие в воде агрессивной углекислоты значительно ухудшает работу очистных сооружений за счет усиленного зарастания отстойников синезелеными водорослями и засорения фильтров пузырьками газа. [4]
Важное значение имеет обеспечение закисной формы Си, поэтому часто добавляют Си и порошке. [5]
Восстанов ление железа в закисную форму началось тотчас же; обра зовавшийся продукт в свою очередь был снова окислен положительными пластинами, что сопровождалось дальнейшим разрядом. Вследствие увеличения скорости сульфатации железо имело разрушительное корродирующее действие на положительные пластины, в особенности поверхностного типа. [6]
Ион окисного железа затем восстанавливается до начальной закисной формы восстановителем. [7]
Когда железо добавляется в электролит в закисной форме, оно окисляется активным материалом положительной пластины до окисного сульфата, причем реакция сопровождается образованием свинцового сульфата и воды. [8]
Железо в травильных ваннах находится обычно в закисной форме. [9]
В природных водах железо содержится, в основном, в закисной форме п может образовывать коллоидальную гидрозакись. [10]
Если в растворе присутствуют ионы окисной ртути, их необходимо восстановить до закисной формы хлоридом олова ( II) или аскорбиновой кислотой. [11]
Если в растворе присутствуют ионы окисной ртути, их необходимо восстановить до закисной формы хлоридом олова ( II) или аскорбиновой кислотой. [12]
Следует отметить, что в присутствии восстановителя, когда железо в основном находится в закисной форме, зависимость десорбции железа от кислотности раствора выражена очень слабо. Следовательно, она связана только со свойствами окисного железа. Кроме того, гидролизованное железо само по себе прочнее связывается с целлюлозой, чем железо, находящееся в ионной форме. [13]
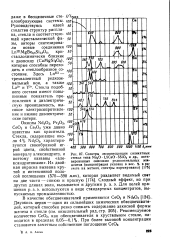 |
Спектры люминесценции силикатных стекол типа NasO 1 5СаО 5SiO2 и др., активированных окислами редкоземельных элементов ( концентрация указана в вес. % в расчете на металл, спектры нормированы. [14] |
N Двуокись церия - один из сильнейших химических обесцвечивателей, который способен резко снижать содержание закисной формы железа в стекле ( см. окислительный ряд, стр. [15]
Страницы: 1 2 3 4