Диссоциация - доломит
Cтраница 2
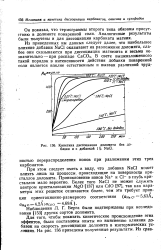 |
Кинетика диссоциации доломита без добавки и с добавкой Р / о NaCl. [16] |
Для того, чтобы показать кинетическое происхождение этих эффектов, были поставлены опыты по выяснению влияния добавок на скорость диссоциации доломита в изотермических условиях. На рис. 136 приведены полученные результаты. [17]
Зона твердофазных реакций, где температура массы повышается до - 650 С, начинаются твердофазные взаимодействия между содой и хромитом и протекает первая стадия диссоциации доломита. [18]
Ниже рассмотрим методику вычисления коэффициентов лишь двух членов: aj e - bl, учитывающего процесс горения топлива, и а / 7 ( /), учитывающего кинетику диссоциации доломита. [19]
Результаты тепловых расчетов [19] показали, что с удовлетворительной точностью можно построить модель, в которой учтены: 1) горение топлива; 2) радиационно-конвективный теплообмен; 3) диссоциация доломита. [20]
Другой прием ускорения разложения доломита заключается во введении в навеску 1 % по весу соли NaCl. При этом температура диссоциации доломита значительно понижается, диссоциация протекает быстрее и при 750 С полностью заканчивается. Наконец, при 1000 - 1100 С происходит выделение углекислого газа как из карбоната кальция доломита, так и из свободного карбоната кальция, не входящего в состав доломита. [21]
Относительно сущности процесса термического разложения доломита существуют различные точки зрения. JII-9 ] указывает, что диссоциация доломита происходит с выделением окиси магния и С02, оставшийся же доломит представляет собою твердый раствор избыточного кальцита и доломита. Третья точка зрения ( С. В. Потапенко [ V-145 ] - для крупнокристаллического доломита) заключается в том, что при нагревании до 750 С наступает распад доломита на свободные карбонаты магния и кальция. Карбонат магния немедленно разлагается с большой скоростью на MgO и С02, так как давление диссоциации при этой температуре близко к 75 атм, а давление диссоциации, равное 1 атм, лежит на 130 - 150 С ниже. Следовательно, в результате частичного разложения доломита при 750 С образуется механическая смесь окиси магния, карбоната кальция и, если процесс не закончился, неразложившегося доломита. [22]
В табл. 4 приведены характеристики образцов доломитов, обожженных при различных температурах. Как видно из таблицы, диссоциация доломитов на отдельные компоненты при 700 С протекает довольно интенсивно. Характерно, что при этой температуре, когда магнезиальный компонент еще не полностью диссоциирован, наблюдается частичная диссоциация кальциевого компонента. В температурном интервале интенсивной диссоциации карбоната кальция получается также распад остатков карбоната магния. Основная масса магнезиального компонента доломита диссоциирует на окись магния и углекислый газ в температурном промежутке 700 - 750 С. [23]
Что касается схемы ( § - А - i), то допускаемая ею возможность предварительного распада доломита на чистые карбонаты аргументируется следующими обстоятельствами. На этом основании справедливо заключают, что первая ступень диссоциации доломита протекает иначе, чем разложение чистого карбоната магния. [24]
Таким образом, установлено, что в температурном промежутке диссоциации магнезиального компонента доломита получается также диссоциация и его кальциевого компонента. Очевидно, что новые твердые фазы, образовавшиеся в результате диссоциации доломита, не в состоянии сразу перейти в стабильное состояние, вследствие чего продукты распада не могут рассматриваться как механическая смесь аморфных или кристаллических веществ. Термическая диссоциация доломита приводит к образованию неустойчивых форм твердой фазы. [25]
 |
Классификация доломитовых пород. [26] |
При изучении условий термической диссоциации доломита необходимо учесть тепловой эффект его образования из карбоната кальция и магния. Работами Байкова [6], Будникова [5] и Берга [7] установлено, что диссоциация доломита в основном протекает в две ступени. [27]
Результаты, полученные при четырех давлениях С02, показывают, что скорость первой ступени диссоциации доломита во много раз меньше, чем для магнезита, и что обе они сильно возрастают с понижением давления. [28]
Если при разложении СаСОз оно осуществляется без особых затруднений в сравнительно короткий срок, то для MgCOa это происходит гораздо медленнее, а при диссоциации доломита равновесия не удается достичь даже в течение нескольких суток. [29]
После решения уравнений всех четырех зон была получена кривая распределения температуры вдоль печи, которая представлена на рис. 5.7. Анализ кривой показывает, что характер температур материала и газа соответствует имеющимся представлениям о процессе: первоначально идет разогрев материала до начала диссоциации доломита; с этого момента процесс нагрева замедляется, после окончания диссоциации наблюдается увеличение скорости нагрева материала до момента достижения максимума, а затем спад температуры. [30]
Страницы: 1 2 3