Геометрическая форма - молекула
Cтраница 3
Заключение об элементах симметрии равновесной конфигурации молекул из колебательной и вращательной структур спектров: Правила отбора для колебательных переходов, связанные с симметрией молекул, могут быть использованы для суждения о симметрии молекул, а следовательно, и о геометрической форме молекул на основании экспериментально наблюдаемых инфракрасных и комбинационных-спектров. Например, при наличии центра симметрии правила отбора показывают, что каждое нормальное колебание может проявляться в виде фундаментальной полосы либо в комбинационном спектре, либо в инфракрасном спектре, либо ни в том, ни в другом. [31]
МО, п, может быть равно 0 1 или 2; е, - энергия / - и МО; q - ядерные координаты; 3) формы МО и порядок их расположения по энергии качественно одинаковы для всех молекул общего структурного типа; 4) если при изменении геометрической формы молекулы увеличивается положительное перекрывание ( перекрывание участков функций АО с одинаковым знаком) между двумя ( или более) АО в составе определенной МО, то энергетический уровень данной МО понижается. [32]
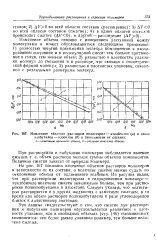 |
Изменение объемов растворов полистирол - этилбе изо л ( о н полп-изоб / тнлен - лзоокган ( 6 с зэвислыости от состава. [33] |
Изменение объема связано с изменением расстояний между молекулами и может обусловливаться следующими причинами: 1) разностью энергий притяжения молекул компонентов в изолированном состоянии и в молекулярной смеси: чем больше притяжение в смеси, тем меньше объем 1 2) разностью в плотностях упаковки молекул до смешения и в растворе, что связано с геометрической формой молекул; 3) разностью в плотностях упаковки, связанном с различными размерами молекул. [34]
Изменение объема связано с изменением расстояний между молекулами и может обусловливаться следующими причинами: 1) разностью энергий притяжения молекул компонентов в изолированном состоянии и в молекулярной смеси: чем больше притяжение в смеси, тем меньше объем; 2) разностью в плотностях упаковки молекул до смешения и в растворе, что связано с геометрической формой молекул; 3) разностью в плотностях упаковки, связанной с различными размерами молекул. [35]
Молекула С2Н4 имеет симметричную плоскую структуру, поэтому в целом молекула С2Н4 неполярна. Геометрическая форма молекул N2H4 и Н2О2 несимметрична и они полярны. Степерь полярности Н2р2 зависит от пространственного расположения частиц HF в димере. [36]
В основе теорий гибридизации и ОЭПВО лежит концепция локализованных МО, приближающая квантовомеханическое описание электронной структуры связей к химическим представлениям. Правильное понимание геометрической формы молекул, принадлежащих к определенным систематическим рядам - АХ г и другим ( НАХ, А3, НААН, НАХ2, Н2АХ), может быть достигнуто и на основании общей теории МО. Необходимо при этом рассмотреть строение канонических МО валентных электронов, получаемых как линейные комбинации АО центрального атома с АО лигандов, и определить, как сказывается переход от одной геометрической структуры к другой на энергетических уровнях каждой отдельной МО. [37]
В таком случае в получаемой эмульсии диспергированным должен быть тот компонент, в сторону которого поверхность раздела вогнута. Исходя из геометрической формы молекул стабилизатора, следовало бы ожидать, что жирные кислоты с длиной углеводородной цепи около 100 А должны стабилизировать эмульсии, в которых размер капель дисперсной фазы имеет тот же порядок. В действительности же оказалось, что размеры капель в эмульсии в сотни раз превышают указанную величину. [38]
Интерес к этим соединениям вызван тем, что они играют значительную роль в теоретической органической химии вследствие ряда особенностей, присущих этому классу соединений. Такими особенностями являются своеобразная геометрическая форма молекулы и вытекающая из нее возможность взаимодействия непосредственно не связанных между собой атомов одной молекулы. Оба эти фактора обусловливают повышенное содержание энергии в средних циклах, которое носит название неклассического конформационного напряжения и является причиной ряда особенностей в химических и физических свойствах. [39]
Представление об электронных парах в молекулах позволяет объяснить валентные углы и конфигурацию молекул. Простой метод определения геометрической формы молекул был предложен Гиллеспи. В основе этого метода лежит модель отталкивания локализованных электронных пар. [40]
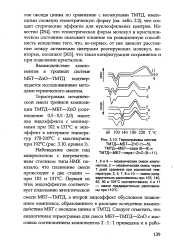 |
Термограммы систем. [41] |
ТМТД, имеющими сложную геометрическую форму ( см. табл. 2.2), что создает стерические эффекты для нуклеофильных центров. Известно [254], что геометрическая форма молекул в кристаллическом состоянии оказывает влияние на реакционную способность вследствие того, что, во-первых, от нее зависит расстояние между активными центрами реагирующих молекул, во-вторых, полагают [303], что такая конфигурация сохраняется и при плавлении кристаллов. [42]
Конечно, внутреннее и внешнее взаимодействия взаимно влияют друг на друга. Наиболее обстоятельно изучено изменение геометрической формы молекулы в результате пространственного отталкивания, что в свою очередь приводит к значительному изменению взаимодействий, передающихся через внешнюю среду. [43]
Направленность химической связи обусловливает геометрическую форму молекул. [44]
Представление об электронных парах в молекулах позволяет объяснить валентные углы и конфигурацию молекул. Простой ме1 тод ( Определения геометрической формы молекул был предложен Гиллеспи. В основе этого метода лежит модель отталкивания локализованных электронных пар. [45]
Страницы: 1 2 3 4