Диссоциация - индикатор
Cтраница 3
Добавление спирта сильно уменьшает константы диссоциации индикаторов, и потому в его присутствии индикаторы, которые ведут себя как кислоты, становятся более чувствительными к ионам водорода, независимо от того, является ли индикатор нувствительным к кислотам или щелочам. Напротив, индикаторы, являющиеся слабыми основаниями, становятся менее нувствительными к ионам водорода. Кроме того, повышение температуры в спиртовых растворах действует в противоположном направлении по сравнению с водными растворами. [31]
Необходимо учесть, что равновесие диссоциации индикаторов устанавливается практически мгновенно; процесс таутомерного превращения поевдокислот и псевдооснований в истинные кислоты и основания протекает во времени, вследствие чего окраска индикаторов не всегда изменяется достаточно быстро. В объемном анализе могут применяться только те индикаторы, перемена окраски которых происходит с достаточной скоростью. [32]
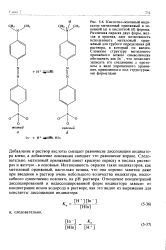
Это изменение окраски связано с диссоциацией индикатора и с изменением его структуры в результате таутомер-ных превращений. [33]
Добавление в раствор кислоты смещает равновесие диссоциации индикатора влево, а добавление основания смещает это равновесие вправо. Следовательно, метиловый оранжевый имеет красную окраску в кислых растворах и желтую - в основных. Интенсивность окраски таких индикаторов, как метиловый оранжевый, настолько велика, что она хорошо заметна даже при введении в раствор очень небольшого количества индикатора, неспособного существенно повлиять на рН раствора. [35]
Поэтому из табличных данных по константам диссоциации индикаторов можно выбрать индикаторы для кислотно-основного титрования любого типа, предельные значения / СИНд для которых установлены в предыдущем разделе. [36]
При колориметрических измерениях пользуются значением константы диссоциации индикаторов, выраженной через концентрации реагирующих веществ, а не через их активности. [37]
Водородный показатель, равный показателю константы диссоциации индикатора, называется точкой перехода. [38]
На этой зависимости между рН раствора и степенью диссоциации индикатора основан другой метод колориметрического определения рН без буферов - метод Михаэлиса с одноцветными индикаторами. [39]
Таким образом, в толковании Кольтгофа, константа диссоциации индикатора является, по существу кажущейся и состоит из произведения истинной константы диссоциации аци-соединения на константу равновесия между аци - и псевдоформами. [40]
Второй раздел объединяет колориметрические методы определения рН и констант диссоциации индикаторов визуально и с помощью фотоэлемента, а также работы по исследованию растворов криоскопическим методом. [41]
 |
Области перехода окраски некоторых индикаторов. [42] |
Значения рН начала и конца перехода определяются значением константы диссоциации индикатора. [43]
Изменение концентрации водородных или гидроксильных ионов сильно влияет на степень диссоциации индикатора. [44]
Концентрация ионов водорода в растворе должна быть численно равна константе диссоциации индикатора. Глаз может уловить изменение окраски раствора только в определенных пределах, а именно тогда, когда не меньше чем 10 % молекул индикаторов диссоциировало на ионы или, наоборот, когда в растворе осталось только 10 % недиссоциированных молекул. Изменение диссоциации за этими пределами не воспринимается глазом. Например, раствор, который содержит только 1 % ионов фенолфталеина ( они красного цвета), будет восприниматься как бесцветный. [45]
Страницы: 1 2 3 4