Диссоциация - карбонат
Cтраница 2
Для процессов диссоциации карбонатов, окислов и сульфидов, где образуются новые твердые фазы, важны именно гетеро-фазные флюктуации. [16]
 |
Зависимость AZ реакции диссоциации MgCO3 от температуры в интервале 600 - 750 К. [17] |
Приведенные примеры диссоциации карбонатов свидетельствуют о том, что при достаточной точности исходных термохимических данных термодинамика дает весьма надежные решения. [18]
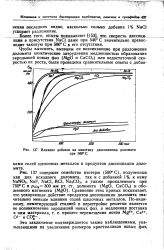 |
Влияние добавок на кинетику диссоциации доломита. [19] |
Механизм и кинетика диссоциации карбонатов, окислов и сульфидов. [20]
На примере реакций диссоциации карбонатов и дегидратации некоторых гидроксидов, твердофазового синтеза силикатов, алюминатов и других тугоплавких веществ была выявлена возможность ускорения соответствующих реакций в пределах от 5 до 300 раз. Об этом свидетельствуют данные, суммированные в табл. 23, а также приведенные в табл. 24, показывающие зависимость степени превращения от продолжительности термообработки в реакциях образования силикатов кальция, являющихся основными минералами портландцементного клинкера. [21]
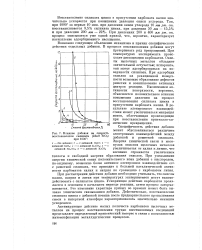 |
Влияние добавок. [22] |
При температурах эксперимента происходит диссоциация карбонатов. Окислы щелочных металлов обладают значительной летучестью; испаряясь, они могут адсорбироваться на поверхности силиката. При адсорбции окислов на реакционной поверхности возможно образование дефектов решетки и возникновение активных центров реакции. Увеличением активности поверхности, вероятно, объясняется положительное влияние повышения давления на процесс восстановления силиката цинка в присутствии карбоната калия. В результате электронного взаимодействия может увеличиваться миграция ионов, облегчающая происходящие при восстановлении кристалло-хи-мические превращения. [23]
Гетерогенные реакции такие, как диссоциация карбонатов, восстановление газами окислов металлов и сульфидов, многие процессы, происходящие при термической обработке стали и сплавов, характеризуются тем, что химические превращения тесно связаны с превращениями в твердом состоянии. В ходе подобных процессов исчезают одни твердые фазы и появляются твердые продукты реакции с другой кристаллической структурой и превращение развивается на поверхности раздела между двумя твердыми фазами - исходным веществом и продуктом реакции. Такие реакции называются топохимическими. Роль поверхностей раздела между фазами была отмечена еще Фарадеем. Он наблюдал, что крупные совершенные кристаллы Na2SO4 - 10 H2O не теряют воду до тех пор, пока на их поверхность не наносится царапина. После этого от образовавшейся границы быстро распространяется процесс выветривания. [24]
Обычно при этой температуре начинается диссоциация карбоната свинца. Незначительный эффект в интервале 600 - 674 обусловлен образованием титанатов свинца и кальция, а эффект при 714 - 774 отвечает, по-видимому, синтезу титаната бария. [25]
Защитные газы образуются за счет диссоциации карбонатов, входящих в состав этих покрытий. Металл, наплавленный электродами с покрытием этой группы, отличается высокой раскисленностью, ire склонен к образованию горячих трещин и содержит большее количество легирующих примесей. Механические свойства наплавленного металла, особенно вязкость и пластичность, очень высокие. [26]
Кроме того, в результате диссоциации карбонатов, входящих в состав покрытия, атмосфера дуги приобретает окислительный характер. [27]
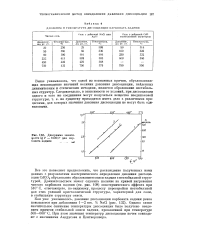 |
Диаграмма зависимости lg P - 1000 / Г для карбоната кадмия. [28] |
Как уже указывалось, давление диссоциации карбоната кадмия резко повышается при добавлении 1 - 2 вес. Однако самое значительное снижение температуры диссоциации было получено введением примеси стабильной окиси кадмия, прокаленной при температуре 500 - 600 С. При этом значения температур диссоциации почти совпадают с значениями Андрусова и Центнершвера. [29]
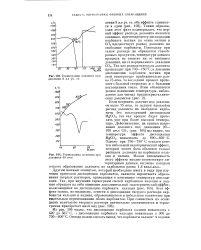 |
Термограмма доломита при давлении 8 мм рт. ст.| Термограмма доломита при давлении 90 атм. [30] |
Страницы: 1 2 3 4 5