Диссоциация - карбонат - кальций
Cтраница 1
Диссоциация карбоната кальция начинается с температуры 700 - 800 С. [1]
Диссоциация карбоната кальция начинается - в зависимости от размера зерен и состояния поверхности - в температурном интервале между 85 и 915 С; но если присутствуют глинозем и кремнезем, она начинается при значительно более низких температурах. [2]
Температура диссоциации карбоната кальция лежит в пределах 850 - 920, ввиду этого механическая прочность гранул при температурах 400 - 600 сохраняется. [3]
Теплота диссоциации карбоната кальция на окись кальция и углекислый газ при 900 С равна 42 56 ккал / моль. [4]
Значение теплоты диссоциации карбоната кальция, которое может быть вычислено на основании многочисленных исследований этой реакции, дает только разность между теплотой образования окиси кальция и карбоната кальция. Поскольку обе эти величины вычисляются из термохимических циклов, включающих теплоту растворения кальция в соляной кислоте ( наименее точный член цикла), такой расчет не может дать независимого значения теплоты образования окиси кальция. [5]
Газовая защита создается диссоциацией карбоната кальция в процессе нагрева и плавления покрытия. В качестве раскислителеп покрытие может содержать ферросилиций, ферромарганец, ферротитан, алюминий. Для легирования металла шва в покрытие могут вводиться металлические порошки. [6]
Преимущества получения диоксида углерода диссоциацией карбоната кальция под действием СВЧ - излучения / / Севергеоэкотех - 2002: Межрегион, молод, науч. [7]
Таким образом, в результате диссоциации карбоната кальция, когда разрушается кристаллическая решетка кристаллов кальцита, получается новое вещество с сильно разрыхленной структурой. Это вещество образовано микрокристаллами окиси кальция. Оно отличается сильно развитой внутренней микропористостью, и поэтому обладает большим избытком энергии. [8]
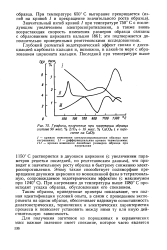 |
Графики, полученные при нагревании образца состава 90 масс. % ZrO2 10 масс. % СаСОз ( в пересчете на СаО. [9] |
Глубокий размытый эндотермический эффект связан с диссоциацией карбоната кальция и, возможно, в какой-то мере с образованием цирконата кальция. [10]
На том же основании, что давление диссоциации карбоната кальция достигает 31 760 мм рт. ст. при 882 С, были предложены две разные схемы прокаливания продукта. Первая заключается в прокаливании оксалата до карбоната кальция в атмосфере двуокиси углерода32 при наиболее приемлемой температуре ниже 882 С. [11]
Удалению двуокиси углерода при такой высокой температуре соответствует диссоциация карбоната кальция до окиси кальция. [12]
При температуре 910 С происходит сильная эндотермическая реакция диссоциации карбоната кальция. Следующая сильная экзотермическая реакция наблюдается между 11ШО и li200 C, причем температура внутри пробы становится заметно более высокой, чем температура печи. При охлаждении легко распознается задержка, отвечающая превращению а-р вновь образовавшегося двукальциевого силиката. Тепловой эффект этого превращения ясно наблюдается также на кривых нагревания смесей, имеющих молекулярные соотношения трехкальциевого силиката. [13]
 |
Давление диссоциации для реакции СаС03 - - СаО С02. [14] |
В таблице 14 приведены давления диссоциации для реакции диссоциации карбоната кальция при различных температурах. [15]
Страницы: 1 2 3 4