Золотой анод
Cтраница 2
Электролиз можно вести с растворимыми золотыми анодами, для чего особенно пригоден электролит 3, или с нерастворимыми из коррозионно-стойкой стали. Анодная плотность тока должна быть в 2 - 3 раза ниже катодной. [16]
Помимо серебра, в золотых анодах обычно присутствуют медь, свинец, висмут, теллур, железо, олово, мышьяк, сурьма, платина, палладий. Механизм растворения такого многокомпонентного сплава очень сложен и далеко не изучен. Медь, значительно более электроотрицательная, чем золото, переходит в раствор, и ее накапливание в электролите после известного предела создает опасность совместного разряда меди и золота. Поэтому при большом содержании меди в анодах ( свыше 2 %) приходится часто менять электролит. [17]
По способу Вольвиля удается растворять золотые аноды, в которых бывает до 200 проб серебра, применяя асимметричный ток. Для этого вместе с постоянным - через ванну пропускают приблизительно равный ему по силе переменный ток. [18]
Корректировка электролитов золочения при пользовании золотыми анодами в основном заключается в систематической добавке цианистого калия. Железистосинеродистый электролит корректируют добавками К4Ре ( С1 Г) 6 и АиС13 по данным анализа. [19]
При электролизе слабо кислого раствора HAuCU золотой анод остается пассивными и на нем выделяется газообразный хлор. [20]
Анодный процесс в щелочных электролитах с золотыми анодами в большой степени зависит от концентрации свободного цианида. При содержании более 3 % KCN выход по току, падает в связи с пассивированием анодов. [22]
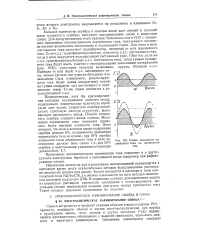 |
Схемы наложения переменного тока на постоянный ток. [23] |
Периодическая, хотя бы кратковременная катодная поляризация золотого анода, содержащего значительные количества серебра не дает шламу хлористого серебра приобретать сплошную липкую структуру, вызывающую пассивность анода. Пленки хлористого серебра спадают с анода слоями. Наложение переменного тока позволяет применять более высокие плотности тока. [24]
Присутствие в электролите ионов натрия вызывает пассивирование золотых анодов вследствие образования на их поверхности труднорастворимой в электролите пассивной пленки. [25]
При золочении в щелочных цианидных электролитах с растворимыми золотыми анодами корректирование производят периодически по результатам анализа раствором дицианоаурата калия ( 100 г / л) и цианида калия ( 500 г / л); при нанесении покрытий золотом и его сплавами из кислых электролитов корректирование по золоту производят через одну-две загрузки; ежедневно корректируют рН электролита введением лимонной или ортофосфор-ной кислоты. [26]
В хлорной кислоте при потенциалах выше 1 4 В золотые аноды пассивируются путем формирования пленки окиси Ai Os. При достаточно высоких плотностях тока может происходить выделение озона, и осаждение Аи ( ОН) 3 сопровождается коррозией золота под осадком с образованием неустойчивой перекиси. Непрерывное выделение на поверхности золота окисла приводит к постепенному повышению пассивности. Анодное поведение платины и некоторых ее сплавов представляет значительный практический интерес, так как эти материалы можно применять в широкой области условий без существенной коррозии, причем условия таковы, что использование других металлов невозможно. [27]
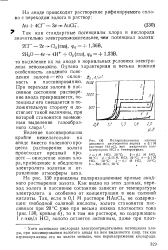 |
Поляризационные анодного растворения золота. [28] |
Хотя потенциал кислорода электроотрицательнее потенциала хлора, при пассивировании золотого анода на нем выделяется хлор, так как перенапряжение его на золоте меньше, чем перенапряжение кислорода. [29]
Электролиз золота можно вести, если содержание серебра в золотых анодах не превышает 200 проб. На практике, однако, стремятся всегда иметь аноды со значительно более низким содержанием второго металла. Это достигается соответствующей шихтовкой материалов, поступающих на приемную плавку. [30]
Страницы: 1 2 3 4